
科目:高中化学 来源: 题型:选择题
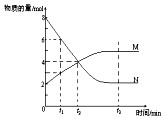 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | 反应的化学方程式为:N═2M | |
| B. | t2时,反应物和生成物的浓度相等,达到平衡 | |
| C. | 当M、N都是气体时增大压强,N物质的量减少 | |
| D. | 升高温度,平衡常数K增大,则反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
下列变化中,属还原反应的是
A.Cl-→Cl2 B.FeCl2→FeCl3 C.C→CO2 D.KMnO4→MnO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学a卷(解析版) 题型:填空题
完成下列表格(注明单位):
微粒 | 摩尔质量 | 质量 | 物质的量 | 微粒数 |
O | 16g/mol | 16g | ||
N2 | 0.5mol | |||
Cu | 64g/mol | 2NA | ||
H2SO4 | 1.5NA |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学a卷(解析版) 题型:选择题
下列叙述中正确的是
A.1molO2的质量是32g·mol-1
B.SO 4 2 - 的摩尔质量为 96 g·mol-1
C.1摩尔任何物质的质量等于该物质的相对分子质量
D.CO2的摩尔质量是44g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学a卷(解析版) 题型:选择题
关于分液漏斗的使用,下列说法正确的是
A.可在分液漏斗内用四氯化碳萃取碘酒中的碘单质
B.放出下层液体时,应打开上方的玻璃塞,并使下端管口紧贴烧杯内壁
C.在分液漏斗中加入萃取剂后应上下颠倒摇匀使萃取剂与溶质充分接触
D.分液漏斗在使用前只需检查旋塞芯处是否漏水即可
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽师大附中高二上10月月考化学卷(解析版) 题型:选择题
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s);△H>0,下列叙述正确的是
Z(g)+W(s);△H>0,下列叙述正确的是
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,一定是n(X)∶n(Y)∶n(Z)=1∶1∶1
C.当容器中气体的平均相对分子质量不变时,一定是v(X)∶v(Y)∶v(Z)=1∶1∶1
D.加入X,上述反应的△H增大
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com