
分析 (1)在某温度下,将H2和I2各0.1mol的气态混合物充入1L的密闭容器中,达到平衡时,测得c(H2)=0.5mol/L,则
H2(g)+I2(g)  2HI(g)
2HI(g)
起始时各物质的浓度(mol•L-1) 1 1 0
各物质的浓度变化量(mol•L-1) 0.5 0.5 1
平衡时各物质的浓度(mol•L-1) 0.5 0.5 1
利用平衡的浓度计算K,K为生成物浓度幂之积与反应物浓度幂之积的比;
(2)设转化的氢气为x,利用三段法得出各物质的平衡浓度,平衡常数与(1)相同,以此来计算;
(3)该反应是放热反应,若升温,平衡逆向移动,据此判断平衡常数的变化;
解答 解:(1)在某温度下,将H2和I2各0.1mol的气态混合物充入1L的密闭容器中,达到平衡时,测得c(H2)=0.5mol/L,则
H2(g)+I2(g)  2HI(g)
2HI(g)
起始时各物质的浓度(mol•L-1) 1 1 0
各物质的浓度变化量(mol•L-1) 0.5 0.5 1
平衡时各物质的浓度(mol•L-1) 0.5 0.5 1
所以K=$\frac{c{\;}^{2}(HI)}{c(H{\;}_{2})•c(I{\;}_{2})}$=$\frac{{1}^{2}}{0.5×0.5}$=4,
故答案为:4;
(2)设转化的氢气为xmol•L-1,利用三段法分析
H2(g)+I2(g)  2HI(g)
2HI(g)
起始时各物质的浓度(mol•L-1) 0.2 0.2 0
各物质的浓度变化量(mol•L-1) x x 2x
平衡时各物质的浓度(mol•L-1) 0.2-x 0.2-x 2x
平衡常数与(1)相同,所以有$\frac{(2x)^{2}}{(0.2-x)(0.2-x)}$=4,解得x=0.1,
所以平衡时[H2]=(0.2-x)mol•L-1=0.1mol•L-1,[HI]=0.2mol•L-1,H2的体积分数为$\frac{0.1}{0.2+0.2}$×100%=25%,平衡时H2的转化率为$\frac{0.1}{0.2}$×100%=50%,
故答案为:0.1;0.2;25%;50%.
(3)该反应是放热反应,若升温,平衡逆向移动,所以平衡常数变小,
故答案为:变小.
点评 本题考查了化学平衡的三段式计算应用,平衡常数的计算分析应用,注意反应前后气体体积不变,同比例增大反应物的量平衡不动,平衡原平衡是等效平衡,题目难度中等.


科目:高中化学 来源: 题型:解答题
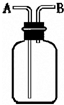 如图所示装置有多种用途,请回答下列问题:
如图所示装置有多种用途,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
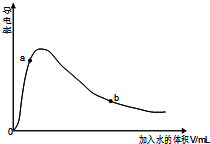 醋酸是中学常用的一种弱酸.
醋酸是中学常用的一种弱酸.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | 向AlCl3溶液中滴加过量的氨水能看到先产生白色沉淀,后沉淀溶解 | |
| C. | 可用浓硫酸或者浓硝酸除去镀在铝表面的铜镀层 | |
| D. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉就会溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠可用作漂白剂和呼吸面具中的供氧剂 | |
| B. | 钠和钾的合金常温下是固体,可用于快中子反应堆作热交换剂 | |
| C. | 碳酸氢钠是焙制糕点所用的发酵粉之一,也可以用于治疗胃酸过多 | |
| D. | 热的碳酸钠溶液可以去除物品表面的油污 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CN-)<c(HCN) | B. | c(HCN)+c(CN-)═0.04 mol/L | ||
| C. | c(OH-)═c(H+)+c(HCN) | D. | c(Na+)>c(CN-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com