
分析 (1)燃烧热是指在25℃、101kPa下,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物的物质的量必须为1mol,产物必须为稳定氧化物;
(2)燃料电池中,燃料在负极失电子发生氧化反应,N2H4失电子生成N2,据此分析书写;
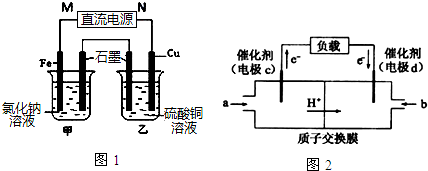
(3)根据通电一段时间后,向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红可知,甲中的石墨极为阴极,则乙中的石墨极为阳极,OH-放电,据此分析pH的变化;本着出来什么就加入什么的原则来分析需要加入的物质;
(4)负极反应式为CH3OH-6e-+H2O=CO2+6H+,正极反应式为O2+4H++4e-=2H2O,按照电极反应式计算.
解答 解:(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热QkJ,则16g甲烷完全燃烧生成二氧化碳和液态水放出的热量为16×QKJ=16QKJ,
则甲烷燃烧热的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-16QKJ•mol-1,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-16QKJ•mol-1;
(2)肼--空气燃料电池是一种碱性电池,该电池放电时,负极是肼燃烧生成氮气和水,负极的电极反应式为:N2H4-4e-+4OH-=N2+4H2O,
故答案为:N2H4-4e-+4OH-=N2+4H2O;
(3)根据通电一段时间后,向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红可知,甲中的石墨极产生了大量的OH-,即为阴极,则乙中的石墨极为阳极,来自于水的OH-放电:2H2O-4e-=4H++O2↑,产生了H+,故溶液的pH变小;乙池中的电解方程式为:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$4Cu+O2↑+2H2SO4,故从电解槽中出来的有铜和氧气,故可以加入CuO,也可以加入CuCO3:CuCO3+H2SO4=CuSO4+H2O+CO2↑,但不能加入Cu(OH)2或Cu2(OH)2CO3,因为含有H元素,会转化为水,使电解质溶液的浓度降低,不能恢复至原浓度,故选AC,故答案为:变小;AC;
(4)负极反应式为CH3OH-6e-+H2O=CO2+6H+,当转移1mol电子时,左侧质量减轻$\frac{1}{6}$×12g=2g,还要有1molH+通过质子交换膜进入右侧,质量减少1g,正极反应式为O2+4H++4e-=2H2O,右侧质量增加32g×$\frac{1}{4}$=8g,加上转移过来的1gH+,因此左右两侧溶液的质量之差为8g+1g+2g+1g=12g,
故答案为:12g.
点评 本题考查较为综合,涉及热化学方程式的书写以及电化学知识,综合考查学生的分析能力和计算能力,把握电极方程式的书写,注意质子交换膜的性质,难度中等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题
 氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g),反应达到平衡后,恢复到反应发生前时的温度.下列有关说法不正确的是( )
如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g),反应达到平衡后,恢复到反应发生前时的温度.下列有关说法不正确的是( )| A. | 根据隔板K滑动与否可判断左右两边的反应是否达到平衡 | |
| B. | 达到平衡后,隔板K最终停留在左侧刻度0--2之间 | |
| C. | 到达平衡时,甲容器中C的物质的量大于乙容器中C的物质的量 | |
| D. | 若平衡时K停留在左侧1处,则活塞停留在右侧5--6之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 普通锌锰干电池中的MnO2在工作时起催化作用 | |
| B. | 若1mol Na2O2与足量水反应产生O2,理论上转移的电子数约为2×6.02×1023 | |
| C. | 室温下,体积、pH均相同的HA和HB两种酸分别与足量的锌反应,HA放出氢气多,说明酸性:HB>HA | |
| D. | 恒温恒压密闭容器中进行的反应N2(g)+3H2(g)?2NH3(g)△H=-a kJ•mol-1,平衡时向容器中再充入一定量NH3,重新达平衡时a值不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 72.4% | B. | 77.8% | C. | 70% | D. | 30% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑤⑧ | B. | ⑤⑦⑧ | C. | ③④⑤⑧ | D. | ②③⑤⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com