
【题目】I.用 98%的浓硫酸(ρ=1.84g/cm3 )配制 1mol/L 稀硫酸 480mL.
(1)实验中应选用的玻璃仪器除了量筒、烧杯、玻璃棒外还需要_____ (填仪器名称)
(2)实验操作:
a.用量筒量取 98%的浓硫酸;
b.将稀释后的浓硫酸转移到容量瓶中;
c.用少量蒸馏水洗涤小烧杯和玻璃棒 2~3 次,并将洗涤液转移到容量瓶中; d.在小烧杯内稀释浓硫酸,稀释时要用玻璃棒不断搅拌; e.向容量瓶中直接加蒸馏水至刻度线 1~2cm 处; f.盖上容量瓶瓶塞,摇匀,装瓶,贴标签;g.用胶头滴管小心加蒸馏水至刻度线;
(3)实验
①步骤 a 中应该取浓硫酸______ mL;
②正确的操作步骤是 _____(填序号).
③下列操作使所配溶液的浓度偏高的有_____ (填字母符号)
A. 使用容量瓶配制溶液时,俯视刻度线定容
B. 取用敞口放置过长时间的浓硫酸
C. 容量瓶用蒸馏水洗净后还剩有少量水
D. 量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶
E. 量取浓硫酸时俯视刻度线
II.某实验小组拟用小颗粒状铝硅合金与足量稀硫酸的反应(已知硅与稀硫酸不反应),测定通常状况(20℃, 101KPa)下的气体摩尔体积.拟选用下列实验装置完成实验:

(1)该小组同学必须选用的装置依次连接的合理顺序为 A、_____.
(2)实验开始时,测量实验中生成 H2 的体积除了上下移动量筒使液面与广口瓶相平,平视读取量筒内 水的体积外,还要注意_____ 。
(3)实验中准确测得 3 个数据:实验前铝硅合金的质量 m1g,实验后残留固体的质量 m2g,实验后量筒中 液面读数为 V mL,则通常状况下气体摩尔体积 Vm= _____L/mol。
【答案】胶头滴管,500mL 容量瓶27.2mLadbcegfADEDG等待锥形瓶恢复至室温再读取体积![]()
【解析】
I.(1)配制480mL溶液,应该选用500mL容量瓶;配制500mL 1mol/L的稀硫酸的步骤有:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,使用的仪器有:50mL量筒、100mL烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以还需要:胶头滴管,500mL 容量瓶;
(3)①98%的浓硫酸(ρ=1.84g/cm3 )的物质的量浓度为:![]() g/mol=18.4mol/L,配制500mL 1mol/L的稀硫酸,需要浓硫酸的体积为:
g/mol=18.4mol/L,配制500mL 1mol/L的稀硫酸,需要浓硫酸的体积为:![]() ≈0.0272L=27.2mL;
≈0.0272L=27.2mL;
②配制500mL 1mol/L的稀硫酸的步骤有:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,故正确的操作步骤是adbcegf;
③A.定容时俯视容量瓶刻度线,导致溶液的体积偏小,则配制的溶液浓度偏高,选项A符合;B. 取用敞口放置过长时间的浓硫酸,浓硫酸吸收空气中的水蒸气浓度变稀,则配制的溶液浓度偏低,选项A不符合;C.因定容时需要加入蒸馏水,故容量瓶用蒸馏水洗净后还剩有少量水,不影响所配制溶液的浓度,选项C不符合;D. 量筒量取溶液后不需要洗涤,故量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶,相当于增加硫酸的量,所配制的溶液浓度偏高,选项D符合;E. 量取浓硫酸时俯视刻度线,所取浓硫酸体积偏小,所配制的溶液浓度偏低,选项E不符合。答案选AD;
II.(1)装置的组装顺序:合金与水反应,用排水量气法测定氢气的体积,其中盛水的试剂瓶导管一定要短进长出,利用增大压强原理将水排出,量筒中水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部,故连接顺序为:E、D、G;
(2)实验开始时,测量实验中生成 H2 的体积除了上下移动量筒使液面与广口瓶相平,平视读取量筒内 水的体积外,还要注意等待锥形瓶恢复至室温再读取体积,以免测得气体体积偏小;
(3)实验前铝硅合金的质量m1 g,实验后残留固体的质量m2 g,则金属铝的质量是m1-m2,实验后量筒中液面读数为VmL,即产生的气体物质的量是![]() ,根据化学反应原理:
,根据化学反应原理:
2Al~3H2↑
2 3
![]()
![]()
解得Vm=![]() LmoL-1。
LmoL-1。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有下列三个反应:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列说法正确的是( )
A. 反应①②③中的氧化产物分别是I2、Fe3+、CoCl2
B. 根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C. 在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
D. 可以推理得到Cl2+FeBr2 =FeCl2+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某氟化稀土样品中氟元素的质量分数,某化学兴趣小组进行如下了实验。
利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量。
实验装置如图所示。

(1)a的作用是____________,仪器d的名称是________________ 。
(2)检查装置气密性:____________(填操作),关闭k,微热c,导管e末端有气泡冒出;停止加热,导管e内有一段稳定的水柱,说明装置气密性良好。
(3)c中加入一定体积高氯酸和mg氟化稀土样品,Z中盛有滴加酚酞的NaOH溶液。加热b、c,使b中产生的水蒸气进入c。
①下列物质可代替高氯酸的是_________(填序号)。
A.硝酸 B.盐酸 C.硫酸 D.磷酸
②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成。若有SiF4生成,实验结果将__________(填“偏高”“ 偏低”或“不受影响”)。
③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是______________。
(4)向馏出液中加入V1mL c1mol·L-1La(NO3)3溶液,得到LaF3沉淀,再用c2mol·L-1EDTA标准溶液滴定剩余La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2ml,则氟化稀土样品中氟的质量分数为______________。
(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏时间),测量并计算出氟元素质量,重复多次。该操作的目的是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,乙为电解饱和MgCl2溶液的装置,其中乙装置中X为阳离子交换膜。用该装置进行实验,反应开始后观察到Fe电极附近出现白色沉淀。下列说法正确的是

A. 甲、乙中电解质溶液的pH都增大
B. 理论上甲中每消耗22.4 L CH4(标准状况下),乙中产生4 mol Cl2
C. 乙中电解MgCl2溶液的总反应为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D. 甲中A处通入CH4,电极反应式为CH4+10OH--8e- =![]() +7H2O
+7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种可用于生物医学领域的平面五角星形钯(Ⅱ)配位络离子结构如右图,已知钯是原子序数为46的过渡元素。
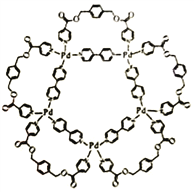
回答下列问题。
(1)钯(Ⅱ)配位络离子中的第二周期元素,其第一电离能从大到小的顺序为_____________(填元素符号)。
(2)钯(Ⅱ)配位络离子中含有的作用力类型为___________ (填序号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(3)钯(Ⅱ)配位络离子中基态钯离子价电子排布式为____________,钯离子的杂化轨道类型_______(填“是”或“不是”)sp3,理由是___________。
(4)钯(Ⅱ)配位络离子中能与氢氧化钠溶液反应的配体,其分子式为__________,每1mol该配体与氢氧化钠反应时断裂的共价键类型及数目为____________。
(5)钯易与亚砜(![]() )生成配合物。当R1和R2都为-CH2C6H5时,三种配合物的结构和键长数据如下:
)生成配合物。当R1和R2都为-CH2C6H5时,三种配合物的结构和键长数据如下:
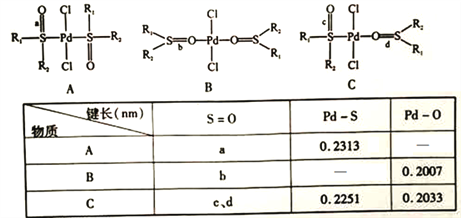
①亚砜的晶体类型为___________________。
②配位键稳定性:Pd-s>Pd-O,其证据为______________ (用上表数据说明)。
③三种配合物中S=O键长不同,其数值最小的是______________(填“a"“b"“c”或“d")
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值, 下列有关叙述正确的是
A. 1 mol OH-所含电子数为10NA
B. 2 L 0.5 mol·L-1Na2SO4溶液中阴离子所带电荷数为0.2NA
C. 标准状况下,1.12 LH2O 含有的氢原子数为0.1NA
D. 14 g由CO和N2组成的混合气体中含有的分子总数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com