
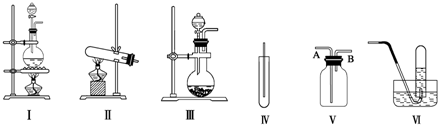
分析 (1)MnO2与浓盐酸反应制取氯气,为固体与液体反应且加热原理,反应生成氯化锰、氯气、水;
(2)2KMnO4+16HCl═2MnCl2+5Cl2↑+8H2O,为固体与液体反应且不加热原理;
(3)根据氯气的性质确定收集方法,注意氯气有毒,不能使氯气逸出污染空气;
(4)利用氯气的密度选择排空气的方法;氯气的氧化性大于碘的氧化性,碘遇淀粉变蓝色.
解答 解:(1)二氧化锰和浓盐酸的反应是固液混合加热型,所以选择Ⅰ装置;在加热条件下,二氧化锰和浓盐酸反应生成氯化锰、氯气和水,反应为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:Ⅰ;MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)KMnO4与浓盐酸的反应是固液混合不需要加热的,所以应选择Ⅲ装置,故答案为:Ⅲ;
(3)氯气有毒,逸出会污染大气,所以不能让氯气逸出;氯气和水能反应是盐酸和次氯酸,盐酸和次氯酸是酸,都能和碱反应,所以可用氢氧化钠溶液吸收氯气,
故答案为:氢氧化钠;防止氯气逸出污染空气;
(4)氯气的密度大于空气的密度,所以应采用向上排空气法收集氯气,故A为进气口;氯气的氧化性大于碘的氧化性,所以氯气能置换出碘化钾中的碘,且碘遇淀粉变蓝色,所以可用湿润的淀粉KI试纸放在B口处检验是否收集满了氯气,
故答案为:A;将湿润的淀粉KI试纸放在B口处,试纸变蓝色,证明氯气已集满.
点评 本题考查常见气体的制备实验及装置,为高频考点,把握实验装置的作用、气体的制备原理为解答的关键,侧重分析与实验能力的考查,注意实验基本技能的综合应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 将100mL 0.1mol•L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.0l NA | |
| B. | Na2O2与足量的水反应生成1 molO2,转移电子数目为2 NA | |
| C. | 某密闭容器中有2mo1SO2和1mol O2,在一定条件下充分反应,转移的电子数为4 NA | |
| D. | 18g重水(D2O)所含的电子数为1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol | B. | 2.5 mol | C. | 3.5mol | D. | 5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子总数 | B. | 原子总数 | C. | 质量 | D. | 质子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4g Mg变成Mg2+时失去的电子数为0.1 NA | |
| B. | 标准状况下,11.2 L水所含的原子数为1.5 NA | |
| C. | 在常温常压下,32g氧气所含原子数目为2NA | |
| D. | 0.1mol/LK2SO4溶液含有 K+0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | a | b | 试管中现象 | 离子方程式 |
| A | 硫酸 | KI淀粉 | 在空气中放置一段时间后溶液呈蓝色 | 4H++4I-+O2═2I2+2H2O |
| B | 稀盐酸 | Na2CO3 | 开始时无气泡,后来有气泡 | CO32-+H+═HCO3-; HCO3-+H+═H2O+CO2↑ |
| C | 稀盐酸 | Na2SiO3 | 产生白色胶状物 | 2H++SiO32-═H2SiO3(胶体) |
| D | 硫酸 | 滴有酚酞的Ba(OH)2 | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合成氨的流程示意图如图:回答下列问题:
合成氨的流程示意图如图:回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com