
”¾ĢāÄæ”æ(1)Š“³öĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬ÓĆĖ«ĻßĒŷرźĆ÷µē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ棬²¢×¢Ć÷”°±»Ńõ»Æ”±”¢”°±»»¹Ō”±”£
¢ŁFe2O3ÓėCOŌŚøßĪĀĻĀµÄ·“Ó¦£ŗ___________________________________”£
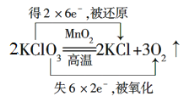
¢ŚKClO3ÓėMnO2ŌŚ¹²ČČĢõ¼žĻĀ·“Ó¦£ŗ________________________________”£
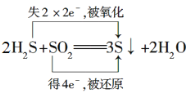
¢ŪH2SĘųĢåŗĶSO2ĘųĢå·“Ó¦Éś³ÉSŗĶĖ®£ŗ______________________________”£
(2)Š“³öĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½£¬²¢ÓƵ„ĻßĒŷرźĆ÷µē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ攣
¢ŁCuŗĶAgNO3ČÜŅŗ·“Ó¦£ŗ________________________________________”£
¢ŚŹµŃéŹŅÖĘCl2µÄ·“Ó¦ĪŖMnO2+4HCl(ÅØ)![]() MnCl2+Cl2”ü+2H2O£ŗ___________________________”£
MnCl2+Cl2”ü+2H2O£ŗ___________________________”£
¢ŪĻņFeCl2ČÜŅŗÖŠĶØČėCl2Éś³ÉFeCl3£ŗ____________________________”£
”¾“š°ø”æ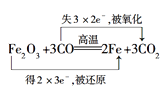
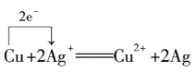
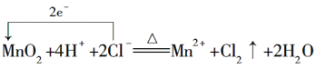
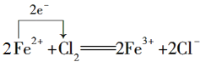
”¾½āĪö”æ
£Ø1£©¢ŁFe2O3ÓėCOŌŚøßĪĀĻĀµÄ·“Ӧɜ³ÉĢśŗĶ¶žŃõ»ÆĢ¼£¬ĘäÖŠŃõ»ÆĢśŹĒŃõ»Æ¼Į£¬µĆµē×Ó£¬±»»¹Ō£¬Ņ»Ńõ»ÆĢ¼ŹĒ»¹Ō¼Į£¬Ź§µē×Ó£¬±»Ńõ»Æ£¬¹Ź“š°øĪŖ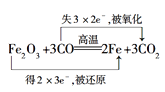 £»
£»
¢ŚKClO3ÓėMnO2ŌŚ¹²ČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČ»Æ¼ŲÓėŃõĘų£¬ĀČĖį¼Ų¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į£¬¹Ź“š°øĪŖ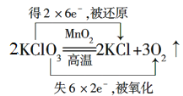 £»
£»
¢ŪH2SĘųĢåŗĶSO2ĘųĢå·“Ó¦Éś³ÉSŗĶĖ®£¬·“Ó¦ÖŠĮņ»ÆĒāŹĒ»¹Ō¼Į£¬Ź§µē×Ó£¬±»Ńõ»Æ£¬¶žŃõ»ÆĮņŹĒŃõ»Æ¼Į£¬µĆµē×Ó£¬±»»¹Ō£¬¹Ź“š°øĪŖ £»
£»
£Ø2£©¢ŁCuŗĶAgNO3·“Ӧɜ³ÉĻõĖįĶŗĶŅų£¬·“Ó¦ÖŠĶĪŖ»¹Ō¼Į£¬ĻõĖįŅųĪŖŃõ»Æ¼Į£¬¹Ź“š°øĪŖ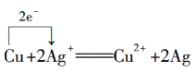 £»
£»
¢ŚŹµŃéŹŅÖĘCl2µÄ·“Ó¦ĪŖMnO2+4HCl£ØÅØ£©![]() MnCl2+Cl2”ü+2H2O£¬·“Ó¦ÖŠHClĪŖ»¹Ō¼Į£¬¶žŃõ»ÆĆĢĪŖŃõ»Æ¼Į£¬¹Ź“š°øĪŖ
MnCl2+Cl2”ü+2H2O£¬·“Ó¦ÖŠHClĪŖ»¹Ō¼Į£¬¶žŃõ»ÆĆĢĪŖŃõ»Æ¼Į£¬¹Ź“š°øĪŖ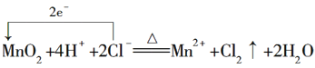 £»
£»
¢ŪĻņFeCl2ČÜŅŗÖŠĶØČėCl2Éś³ÉFeCl3£¬·“Ó¦ÖŠFeCl2ŹĒ»¹Ō¼Į£¬ĀČĘųŹ§Ńõ»Æ¼Į£¬¹Ź“š°øĪŖ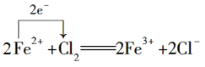 ”£
ӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ®ŹĒÉśĆüÖ®Ō“£¬ĖüÓėĪŅĆĒµÄÉś»īĆÜĒŠĻą¹Ų”£×ŌĄ“Ė®³§³£ÓĆøßĢśĖįÄĘ(Na2FeO4)øÄÉĘĖ®ÖŹ”£øßĢśĖįÄĘ¾ßÓŠŗÜĒæµÄŃõ»ÆŠŌ£¬ŹĒŅ»ÖÖŠĀŠĶµÄĀĢÉ«¾»Ė®Ļū¶¾¼Į£¬ŌŚ¹¤ŅµÉĻÖʱøøßĢśĖįÄʵķ½·ØÓŠ¶ąÖÖ”£
£Ø1£©¼ņŹöøßĢśĖįÄĘÓĆӌɱ¾śĻū¶¾Ķ¬Ź±ÓÖĘšµ½¾»Ė®×÷ÓƵÄŌĄķ_________________________________________________________________________”£
£Ø2£©øÉ·ØÖʱøøßĢśĖįÄʵķ“Ó¦ŌĄķČēĻĀ£ŗ
2FeSO4+6Na2O2==aNa2FeO4+bMӟ+2Na2O+2Na2SO4
¢ŁøßĢśĖįÄĘÖŠĢśŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ________________”£
¢ŚÉĻŹö·½³ĢŹ½ÖŠb=____”£ĆæÉś³É1molM£¬øĆ·“Ó¦×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ_____________mol”£
£Ø3£©¹¤ŅµÉĻæÉŅŌĶعż“ĪĀČĖįÄĘŃõ»Æ·ØÖʱøøßĢśĖįÄĘ£¬Éś²ś¹ż³ĢČēĻĀ£ŗ
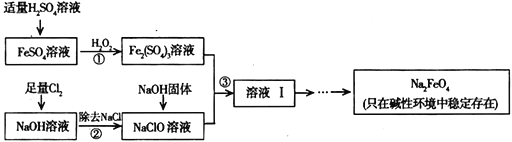
¢Ł²½Öč¢ŪÖŠ³żÉś³ÉNa2FeO4Ķā£¬»¹ÓŠø±²śĘ·Na2SO4”¢NaCl£¬Ōņ²½Öč¢ŪÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________________________________”£
¢Ś¼ŗÖŖNa2FeO4ŌŚĒæ¼īŠŌČÜŅŗÖŠµÄČܽā¶Č½ĻŠ””£æÉĻņNa2FeO4ČÜŅŗÖŠ¼ĢŠų¼ÓČėĒāŃõ»ÆÄĘ¹ĢĢåµĆµ½Šü×ĒŅŗ”£“ÓNa2FeO4Šü×ĒŅŗµĆµ½¹ĢĢåµÄ²Ł×÷Ćū³ĘĪŖ_____________________”£
£Ø4£©¼ĘĖćNa2FeO4µÄĻū¶¾Š§ĀŹ£ØŅŌµ„Ī»ÖŹĮæµĆµ½µÄµē×ÓŹż±ķŹ¾£©Ō¼ŹĒĀČĘųµÄ_______±¶(½į¹ū±£ĮōĮ½Ī»Š”Źż”£)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠČĖČĻĪŖŌŖĖŲÖÜĘŚ±ķÖŠĪ»ÓŚ¢ńA×åµÄĒāŌŖĖŲ£¬Ņ²æÉŅŌ·ÅŌŚ¢÷A×壮ĻĀĮŠĪļÖŹÖ§³ÖøĆ¹ŪµćµÄŹĒ£Ø £©
A.HF
B.H3O+
C.NaH
D.H2O2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ŌŚ25 ”ęĻĀ£¬ĻņÅØ¶Č¾łĪŖ0.1 mol”¤L£1µÄMgCl2ŗĶCuCl2»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČė°±Ė®£¬ĻČÉś³É________³Įµķ(Ģī»ÆѧŹ½)£¬Éś³ÉøĆ³ĮµķµÄĄė×Ó·½³ĢŹ½ĪŖ___________”£ŅŃÖŖ25 ”ꏱKsp[Mg(OH)2]£½1.8”Į10£11£¬Ksp[Cu(OH)2]£½2.2”Į10£20”£
£Ø2£©ĻņBaCl2ČÜŅŗÖŠ¼ÓČėAgNO3ŗĶKBr£¬µ±Į½ÖÖ³Įµķ¹²“ꏱ£¬![]() £½________”£[Ksp(AgBr)£½5.4”Į10£13£¬Ksp(AgCl)£½2.0”Į10£10]
£½________”£[Ksp(AgBr)£½5.4”Į10£13£¬Ksp(AgCl)£½2.0”Į10£10]
£Ø3£©ŅŃÖŖFe(OH)3µÄČܶȻż³£ŹżKsp£½1.1”Į10£36”£ŹŅĪĀŹ±ŌŚFeCl3ČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ£¬µ±ČÜŅŗpHĪŖ3Ź±£¬Ķعż¼ĘĖćĖµĆ÷Fe3£«ŹĒ·ń³ĮµķĶźČ«_______________________”£(ĢįŹ¾£ŗµ±Ä³Ąė×ÓÅØ¶ČŠ”ÓŚ10£5 mol”¤L£1Ź±æÉŅŌČĻĪŖøĆĄė×Ó³ĮµķĶźČ«)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
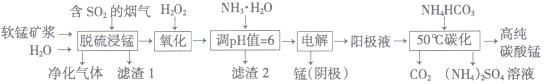
”¾ĢāÄæ”湤ŅµÉĻĄūÓĆČķĆĢæó½¬ŃĢĘųĶŃĮņĪüŹÕŅŗÖĘČ”µē½āĆĢ£¬²¢ĄūÓĆŃō¼«ŅŗÖʱøøß“æĢ¼ĖįĆĢ”¢»ŲŹÕĮņĖįļ§µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ØČķĆĢæóµÄÖ÷ŅŖ³É·ÖŹĒMnO2£¬»¹ŗ¬ÓŠ¹č”¢Ģś”¢ĀĮµÄŃõ»ÆĪļµČŌÓÖŹ£©£ŗ
ŅŃÖŖ£ŗFe(OH)3µÄKsp=l.0”Į10-38£¬Al(OH)3µÄKsp=1.0”Į10-34
£Ø1£©Ņ»¶ØĪĀ¶ČĻĀ£¬ ”°ĶŃĮņ½žĆĢ”±Ö÷ŅŖ²śĪļĪŖMnSO4£¬Éś³ÉøĆ²śĪļµÄ»Æѧ·½³ĢŹ½ĪŖ_________”£
£Ø2£©³£ĪĀĻĀ£¬µ÷½ŚpH=6Ź±£¬µĆµ½µÄ”°ĀĖŌü2”±Ö÷ŅŖ³É·ÖĪŖFe(OH)3ŗĶ_____£Ø»ÆѧŹ½£©£¬“ĖŹ±ČÜŅŗÖŠµÄFe3+ĪļÖŹµÄĮæÅضČĪŖ_________ ”£
£Ø3£©”°µē½ā”±Ź±ÓƶčŠŌµē¼«£¬Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖ_______________”£
£Ø4£©”°50”ęĢ¼»Æ”±µĆµ½øß“æĢ¼ĖįĆĢ£¬·“Ó¦µÄĄė×Ó·½³ĢĪäĪŖ____________________”£”°50”ęĢ¼»Æ”±Ź±¼ÓČė¹żĮæNH4HCO3£¬æÉÄܵÄŌŅņ£ŗ¢ŁŹ¹MnSO4³ä·Ö×Ŗ»ÆĪŖMnCO3£»¢Ś________________£»¢Ū________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜÖü“ęŌŚ“ųÄ„æŚČūµÄ²£Į§ŹŌ¼ĮĘæÖŠµÄŹŌ¼ĮŹĒ£Ø £©
A.KOHČÜŅŗ
B.ÅØH2SO4
C.Ė®²£Į§
D.Ēā·śĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃõ»Æ»¹Ō·“Ó¦ŹĒŅ»ĄąÖŲŅŖµÄ·“Ó¦£¬Ēė°“ŅŖĒóĶź³ÉĻĀĮŠĢāÄ攣
(1)¶Ō·“Ó¦NH3+O2”Ŗ”ŖNO+H2O(Ī“ÅäĘ½)×÷·ÖĪö£¬²¢ÓƵ„ĻßĒŷرź³öµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæ£ŗ_____________”£øĆ·“Ó¦ÖŠ£¬________ŹĒ»¹Ō¼Į£¬________ŹĒ»¹Ō²śĪļ£¬±»»¹ŌµÄĪļÖŹŹĒ________”£
(2)ŌŚŅ»¶ØĢõ¼žĻĀ£¬·“Ó¦2NH3+3CuO![]() 3Cu+N2+3H2OÄÜĖ³Ąū½ųŠŠ£¬¶Ō“Ė·“Ó¦µÄ·ÖĪöŗĻĄķµÄŹĒ________”£
3Cu+N2+3H2OÄÜĖ³Ąū½ųŠŠ£¬¶Ō“Ė·“Ó¦µÄ·ÖĪöŗĻĄķµÄŹĒ________”£
¢ŁøĆ·“Ó¦ŹĒÖĆ»»·“Ó¦
¢Ś·“Ó¦ÖŠNH3±»Ńõ»ÆĪŖN2
¢ŪŌŚ·“Ó¦ÖŠĢåĻÖĮĖ½šŹōĶµÄ»¹ŌŠŌ
¢ÜŌŚ·“Ó¦ÖŠĆæÉś³É1 mol H2O×ŖŅĘ1 molµē×Ó
(3)ŌŚ·“Ó¦2H2S+SO2![]() 3S+2H2OÖŠ±»Ńõ»ÆµÄŌŖĖŲÓė±»»¹ŌµÄŌŖĖŲµÄÖŹĮæ±ČĪŖ ________”£
3S+2H2OÖŠ±»Ńõ»ÆµÄŌŖĖŲÓė±»»¹ŌµÄŌŖĖŲµÄÖŹĮæ±ČĪŖ ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀĢśæÉŅŌŗĶCO2·¢Éś·“Ó¦£ŗFe(s)+CO2(g) ![]() FeO(s)+CO(g)£»”÷H>0
FeO(s)+CO(g)£»”÷H>0
£Ø1£©Ņ»¶ØĪĀ¶ČĻĀ£¬ĻņijĆܱÕČŻĘ÷ÖŠ¼ÓČė×ćĮæĢś·Ū²¢³äČėŅ»¶ØĮæµÄCO2ĘųĢ壬·“Ó¦¹ż³ĢÖŠCO2ĘųĢåŗĶCOĘųĢåµÄÅضČÓėŹ±¼äµÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾£¬Ōņ8·ÖÖÓÄŚCOµÄĘ½¾ł·“Ó¦ĖŁĀŹv(CO)=______”£

£Ø2£©Š“³öøĆ·“Ó¦Ę½ŗā³£±ķ“ļŹ½£ŗK=__________£»ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹øĆ·“Ó¦µÄĘ½ŗā³£ŹżKŌö“óµÄŹĒ____£ØĢīŠņŗÅ£©”£
A£®ÉżøßĪĀ¶Č B£®Ōö“óŃ¹Ēæ C£®³äČėCO D£®ŌŁ¼ÓČėŅ»Š©Ģś·Ū
£Ø3£©·“Ó¦“ļµ½Ę½ŗāŗó£¬Čō±£³ÖČŻĘ÷Ģå»ż²»±äŹ±£¬ŌŁĶØČėÉŁĮæµÄCO2£¬ŌņCO2µÄ×Ŗ»ÆĀŹ½«______ £ØĢī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±£©”£
£Ø4£©ĢśµÄÖŲŅŖ»ÆŗĻĪļŌŚÉś²śÉś»īÖŠÓ¦ÓĆŹ®·Ö¹ć·ŗ”£
¢ŁøßĢśĖįÄĘ(Na2FeO4)ŹĒŅ»ÖÖŠĀŠĶŅūÓĆĖ®Ļū¶¾¼Į”£øßĢśĖįÄĘÉś²ś·½·ØÖ®Ņ»ŹĒ£ŗĒæ¼īŠŌČÜŅŗÖŠÓĆNaClOŃõ»ÆFe(OH)3Éś³ÉøßĢśĖįÄĘ”¢ĀČ»ÆÄĘŗĶĮķŅ»ÖÖ³£¼ū»ÆŗĻĪļ£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________”£
¢ŚøßĢśµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
ĻĀĮŠŠšŹö“ķĪóµÄŹĒ____£ØĢīŠņŗÅ£©”£
A£®·ÅµēŹ±Ćæ×ŖŅĘ6molµē×Ó£¬øŗ¼«ÓŠ2mol K2FeO4±»»¹Ō
B£®³äµēŹ±Ņõ¼«·“Ó¦ĪŖ£ŗZn(OH)2 +2e-=Zn+ 2OH-
C£®·ÅµēŹ±Õż¼«·“Ó¦ĪŖ£ŗFeO42-+ 3e-+ 4H2O= Fe(OH)3+ 5OH-
D£®³äµēŹ±Ńō¼«ø½½üČÜŅŗµÄ¼īŠŌ¼õČõ
£Ø5£©ŅŃÖŖ£ŗ2CO(g)+O2(g)= 2CO2(g) ”÷H=-566 kJ/mol
2H2(g)+ O2(g)= 2H2O(g)£»”÷H=-483.6 kJ/mol
Š“³öCOŗĶH2O(g)×÷ÓĆÉś³ÉCO2ŗĶH2µÄČČ»Æѧ·½³ĢŹ½£ŗ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜŌŚČÜŅŗÖŠ“óĮæ¹²“ęµÄŅ»×éĄė×ÓŹĒ£Ø £©
A.Cu2+”¢SO42-”¢OH”Ŗ”¢K+B.Na+”¢CO32-”¢H+”¢Cl-
C.H+ӢCl-ӢNO3-ӢBa2+D.Ca2+ӢH+ӢCO32-ӢNO3-
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com