
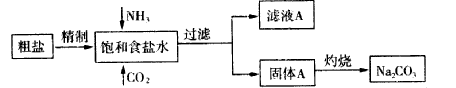
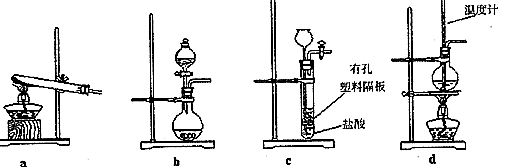


科目:高中化学 来源:不详 题型:单选题
| A.金属钠保存在煤油中 |
| B.钠的密度比水小 |
| C.钠在空气中燃烧生成Na2O |
| D.实验时用剩的钠块应该放回原试剂瓶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
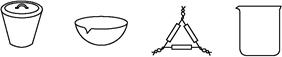
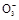
 BaCO3↓+H2O)
BaCO3↓+H2O)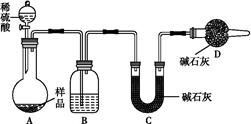
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
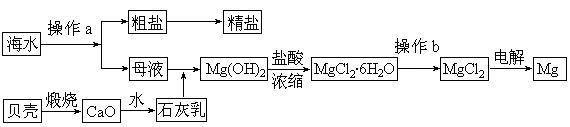
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
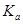 如下表:
如下表: | H2CO3 | Ka1=4.3×10-7 | H2C2O4 | Ka1=5.6×10-2 |
| Ka2=5.6×10-11 | Ka2=5.42×10-5 |
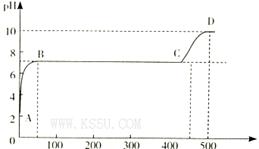
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将浓硝酸保存在无色玻璃瓶中 |
| B.金属钠和钾保存在煤油中 |
| C.Na2CO3可以保存在玻璃塞的玻璃瓶中 |
| D.NaOH固体放在滤纸上称量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al和氢氧化钠溶液 | B.NaOH和CO2 |
| C.Na和O2 | D.AlCl3和NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com