
【题目】下列各组离子中,能在强酸性透明溶液中大量共存的是( )
A.Na+、K+、SO42-、OH-B.Na+、K+、Cl-、HCO3-
C.Na+、Cu2+、Cl-、SO42-D.NH4+、Ca2+、NO3-、CO32-
科目:高中化学 来源: 题型:
【题目】利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的制备流程如下:

(1)“酸溶”时,Fe2O3与硫酸反应的化学方程式为____。
(2)滤渣I的主要成分是FeS2、S和______(填化学式);Fe3+被FeS2还原的离子方程式为______。
(3)“氧化”中,生成FeOOH的离子方程式为_______________。
(4)滤液II中溶质是Al2(SO4)3和______(填化学式):“洗涤”时,检验铁黄表而已洗涤干净的操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气.为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,反应装置略去).
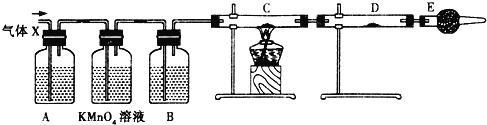
注:C中为氧化铜粉末,试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为:________________________________;
(2)乙同学认为还可能产生氢气的理由是:____________________________________;
(3)丙同学在安装好装置后,必不可少的一步操作是:__________________________;
(4)A中试剂是______,D中试剂是______;
(5)E装置的作用是_________________________;
(6)可以证明气体X中含有氢气的实验现象是:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A是农药生产中的一种中间体,其结构简式如图所示. 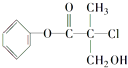
由A的结构推测,它能(填字母).
a.使溴的四氯化碳溶液褪色
b.使酸性KMnO4溶液褪色
c.和稀硫酸混合加热,可以发生取代反应
d.与Na2CO3溶液作用生成CO2
e.1mol A和足量的NaOH溶液反应,最多可以消耗3mol NaOH
f.和NaOH醇溶液混合加热,可以发生消去反应
g.1mol A和足量的H2反应,最多可以消耗4mol H2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于“物质的量”“摩尔”和“摩尔质量”的叙述正确的是
A. “物质的量”是国际单位制中的个基本单位
B. 1mol任何物质均约含有6.02×1023个分子
C. 物质的摩尔质量等于其相对分子质量或相对原子质量
D. 0.012kg12C中所含的碱原子数为NA(NA代表阿伏加德罗常数的数值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中可逆反应mA(g)+nB(g) ![]() pC(g)+qQ(g) 当m、n、p、q为任意整数且C为有色物质,可逆反应一定达到平衡的标志是 ( )
pC(g)+qQ(g) 当m、n、p、q为任意整数且C为有色物质,可逆反应一定达到平衡的标志是 ( )
①混合气体的平均摩尔质量不再改变 ②体系的温度不再改变③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率VA:VB:VC:VQ=m:n:p:q ⑥体系颜色不再变化
⑦单位时间内m mol A断键反应,同时p mol C也断键反应
A. ②③④⑤⑥ B. ①②③④⑤ C. ②③④⑥⑦ D. ①②③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2→CCl3CHO+5HCl可能发生的副反应是C2H5OH+HCl→C2H5Cl+H2O。某探兖小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。回答下列问题:

(1)仪器a的名称是______________。
(2)装置A中发生反应的离子方程式为____________________________________。
(3)仪器b中冷凝水从______(填“p”或“q”,下同)口进,___________口出。
(4)若撤去装置B,对实验的影响是__________________________________________________。
(5)实验时发现D中导管口处气泡速率过快,合理的解决方法是______________________。
(6)已知:CCl3CHO+OH-→CHCl3+HCOO-;HCOO-+I2-=H++2I-+CO2↑;I2+2S2O32-=2I-+S4O62-。称取0.40g产品,配成待测溶液,加入20.00mL0.100mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00mL。滴定时所用指示剂是__________________________,达到滴定终点的现象是_____________________________________________________,测得产品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定的环境中一定能大量共存的是 ( )
A. 滴加石蕊试液显红色的溶液:Fe3+、NH![]() 、Cl-、SCN-
、Cl-、SCN-
B. 加入铝粉能产生H2的溶液:NH![]() 、Fe2+、SO
、Fe2+、SO![]() 、NO
、NO![]()
C. 含有大量HCO![]() 的溶液:NH
的溶液:NH![]() 、Ca2+、Mg2+、I-
、Ca2+、Mg2+、I-
D. 含有大量ClO-的溶液:H+、Mg2+、I-、SO![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com