
| A. | 悬浮物由黑色变为白色,因SO2是一种漂白剂 | |
| B. | 悬浮物由黑色变为白色,因为形成了PbSO4 | |
| C. | 有黄色沉淀生成 | |
| D. | 有臭鸡蛋味的气体放出 |
分析 四价铅有强氧化性,能跟盐酸反应生成氯气四价铅氧化性大于氯气,氯气能氧化二氧化硫,则二氧化铅能氧化二氧化硫,将SO2通入悬浮着黑色PbO2的热水中,发生的反应为SO2+PbO2=PbSO4↓,据此分析解答.
解答 解:四价铅有强氧化性,能跟盐酸反应生成氯气四价铅氧化性大于氯气,氯气能氧化二氧化硫,则二氧化铅能氧化二氧化硫,将SO2通入悬浮着黑色PbO2的热水中,发生的反应为SO2+PbO2=PbSO4↓,该反应中二氧化硫体现还原性、二氧化铅体现氧化性,硫酸铅为白色沉淀,所以悬浮物由黑色变为白色,故选B.
点评 本题以二氧化硫为载体考查氧化还原反应,为高频考点,侧重考查学生分析判断及知识运用能力,明确反应实质是解本题关键,题目难度不大.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:解答题
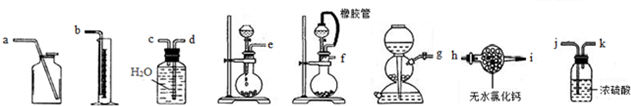
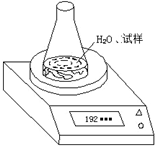
| 锥形瓶+水+试样 | |||||
| 读数次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 质量/g | 192.80 | 192.30 | 192.10 | 192.00 | 192.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每一周期元素都是从碱金属开始,以稀有气体结束 | |
| B. | f区都是副族元素,s区和p区的都是主族元素 | |
| C. | 铝的第一电离能小于K的第一电离能 | |
| D. | B电负性和Si相近 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
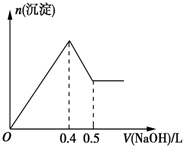 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 6:1 | B. | 2:3 | C. | 1:3 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 甲 | 乙 |
| A | 溴乙烷水解制备乙醇 | 乙烯水化制备乙醇 |
| B | 甲烷与氯气反应制备四氯化碳 | 乙烯通入KMnO4溶液中 |
| C | 甲苯与KMnO4溶液反应生成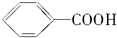 | 苯与液溴反应制备溴苯 |
| D | 蛋白质水解得到氨基酸 | 乙醇与冰醋酸反应生成乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 | |
| B. | 浓硫酸沾在皮肤上时应用大量水冲洗,再涂上3%~5%的NaOH溶液 | |
| C. | 实验室进行蒸馏操作时若忘加了沸石,应停止反应冷却至室温后再加入 | |
| D. | 配制硫酸溶液时,可先在量筒中加一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇所含的分子数为NA | |
| B. | 1mol/LCaCl2溶液中含有的氯离子数目为2NA | |
| C. | 1 mol金属钠在足量乙醇完全反应转移的电子数为2NA | |
| D. | 1.6g 甲烷中含有的电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com