
对于可逆反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ,下列叙述正确的是
4NO(g)+6H2O(g) ,下列叙述正确的是
A. 达到化学平衡状态时,4v正(O2)=5V逆(NO)
B. 化学反应速率的关系为2V正(NH3)=3V正(H2O)
C. 达到化学平衡状态时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到化学平衡状态
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源:2015-2016学年黑龙江省高二上期末化学卷(解析版) 题型:推断题
(1)X是最简单的烯烃。现有如下的反应关系:(已知F是一种常见的塑料)
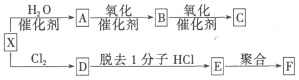
①X的结构简式为 ;C的官能团名称是 。
②由E制取F的化学方程式为 。
(2)某实验小组用下列装置进行A转化为B的实验。
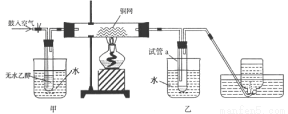
①请写出A制取B的化学反应方程式:___________________________。
②甲和乙两个水浴作用不相同。甲的作用是_____________;乙的作用是_____________。
③试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,要除去该物质,可在混合液中加入___(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
(3)阿斯匹林的结构简式为: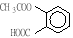 ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为 。
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为 。
(4)某烃的分子式为C8H10,其不能使溴水褪色,但可使酸性KMnO4溶液褪色,且此烃与液溴在催化剂条件下只得到一种取代产物,其结构可能有 种。
A.1种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一上学期12月月考化学试卷(解析版) 题型:填空题
(1)CCl4和蒸馏水都是无色液体,请按下列要求用实验方法鉴别之(简要地写出实验过程)
① 只允许用一种试剂________________
② 不用任何试剂________________
(2)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁任城区高二上学期统考化学试卷(解析版) 题型:选择题
下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是
A.增大反应物的浓度,活化分子百分数增加,反应速率加快
B.增大气体反应的压强,单位体积中活化分子数增多,气体反应速率加快
C.升高温度能使化学反应速率增大,主要原因是增加了活化分子的百分数,从而使有效碰撞频率提高
D.催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高一上12月阶段测化学试卷(解析版) 题型:选择题
将过量的CO2分别通入下列溶液中,最终有沉淀析出的溶液是
①CaCl2溶液 ②Na2SiO3溶液 ③Ca(ClO)2溶液 ④饱和Na2CO3溶液
A.①②③④ B.只有②④ C.只有①②③ D.只有②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省平度市高一上学期直升班抽考化学试卷(解析版) 题型:选择题
下列物质中属于电解质,且能导电的是
A.熔融的氢氧化钾 B.液态铜
C.液态氯化氢 D.固态氯化钾
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学情调查化学试卷(解析版) 题型:选择题
下列有关实验的说法正确的是
A.用干燥的pH试纸测定新制氯水的pH
B.中和滴定实验中,洗净后的锥形瓶不需要干燥
C.用Na2S溶液与AlCl3溶液混合制取Al2S3
D.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期期末理综化学试卷(解析版) 题型:填空题
工业生产硝酸铵的流程如下图所示:

(1)硝酸铵的水溶液呈 (填“酸性”、“中性”或“碱性”);其水溶液中各离子的浓度大小顺序为 。
(2)已知N2(g)+3H2(g) 2NH3(g) △H < 0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。
2NH3(g) △H < 0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。

①曲线a对应的温度是 。
②关于工业合成氨的反应,下列叙述正确的是 。
A.及时分离出NH3可以提高H2的平衡转化率
B.P点原料气的平衡转化率接近100%,是当前工业生产工艺中采用的温度、压强条件
C.上图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
D.M点比N点的反应速率快
E.如果N点时c(NH3)=0.2 mol·L-1,N点的化学平衡常数K ≈ 0.93 L2/mol2
(3)尿素[ CO(NH2)2 ]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272 kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138 kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式: 。
(4)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下左图所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________步反应决定,总反应进行到_________min时到达平衡。
②在上右图中画出第二步反应的平衡常数K随温度的变化的示意图。
(5)电解尿素[ CO(NH2)2 ]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为______________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州港经济开发区中学高二上12月月考化学试卷(解析版) 题型:选择题
从人类生存的环 境考虑,未来理想的燃料应是
境考虑,未来理想的燃料应是
A.煤 B.氢气 C.石油炼制品 D.酒精
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com