
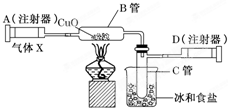
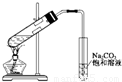
 如图所示的实验装置可用来测定含两种元素的某种气体x的分子式.在注射器A中装有240mL气体X慢慢通过 不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到下面的实验结果:实验前B管重20.32g,实验后B管重20.00g,B管中的黑色粉末变成红色粉末.在C管中收集的无色液体是水;在注射器D中收集的气体是氮气.试回答下列问题:
如图所示的实验装置可用来测定含两种元素的某种气体x的分子式.在注射器A中装有240mL气体X慢慢通过 不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到下面的实验结果:实验前B管重20.32g,实验后B管重20.00g,B管中的黑色粉末变成红色粉末.在C管中收集的无色液体是水;在注射器D中收集的气体是氮气.试回答下列问题:
| ||
| ||
| 240mL |
| 24000mL |
| 0.28g |
| 28g/mol |
| 0.32g |
| 16g/mol |
| 0.32g |
| 0.01mol |
| ||
| ||


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
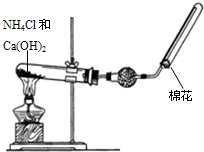 某同学在实验室用如图所示的实验装置制取并收集干燥的氨气.请回答下列问题.
某同学在实验室用如图所示的实验装置制取并收集干燥的氨气.请回答下列问题.
| ||
| ||
| ||
| 高温高压 |
| ||
| 高温高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.淀粉遇碘变蓝,因此可用碘化钾溶液检验淀粉的存在 |
| B.碘易溶于乙醇等有机溶剂,因此可用乙醇萃取碘水中的碘 |
| C.用溴水鉴别苯、乙醇、四氯化碳 |
D.用如图所示的实验装置可制取少量乙酸乙酯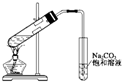 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山西省阳泉十五中高一(下)月考化学试卷(5月份)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com