
分析 乙烯含有碳碳双键,可发生加成、加聚和氧化反应,可用作催熟剂;
乙醇可使蛋白质变性,可用作消毒剂;
乙醛含有醛基,可与新制Cu(OH)2悬溶液发生氧化还原反应,以此解答该题.
解答 解:乙醛含有醛基,可与新制Cu(OH)2悬溶液发生氧化还原反应,结构简式为CH3CHO,可作果实催熟剂的是乙烯,结构简式为CH2=CH2,可在医疗上用作消毒剂的是乙醇,分子式为C2H6O,
故答案为:CH3CHO;CH2=CH2;C2H6O.
点评 本题考查有机物的组成、性质和用途,为高频考点,侧重考查学生的分析能力,有利于培养学生良好的科学素养,本题注意把握有机物的官能团的结构和性质,把握官能团,是学习有机化学的关键,学习中注意积累,难度不大.


科目:高中化学 来源: 题型:解答题
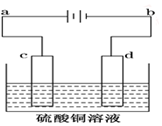 电解装置如图所示:
电解装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
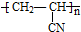 )混合物制作而成的复合材料.工业上用氧化铝电解冶铝的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;聚丙烯腈单体分子中位于同一平面的原子数目最多为7个.
)混合物制作而成的复合材料.工业上用氧化铝电解冶铝的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;聚丙烯腈单体分子中位于同一平面的原子数目最多为7个.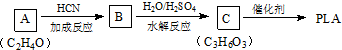
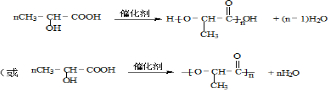 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率增大 | ||
| C. | 物质C的质量分数增大 | D. | m>2n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75mL2mol•L-1 CaCl2溶液 | B. | 150mL2mol•L-1NaCl溶液 | ||
| C. | 150mL2mol•L-1KClO3溶液 | D. | 75mL1mol•L-1 AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,CuS的溶解度大于ZnS的溶解度 | |
| B. | 25℃时,向含有等物质的量的FeCl2、CuCl2的混合液中逐滴加入Na2S,最先出现沉淀的是FeS | |
| C. | 除去ZnCl2溶液中的Cu2+,可以选用FeS作沉淀剂 | |
| D. | 将足量CuSO4溶解在0.1 mol/L的H2S溶液中,S2-能达到的最大浓度为$\sqrt{1.3}$×10-18mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com