
【题目】(12分)溴苯是一种常用的化工原料,通常以苯和溴为原料制取,查资料知:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
在水中的溶解度 | 微溶 | 微溶 | 微溶 |
实验室制备溴苯的实验步骤如下:
步骤1:在a中加入15 mL苯和少量铁屑,再将b中4.0 mL液溴慢慢加入到a中。
步骤2:充分反应后,向a中加入10 mL水,然后过滤除去未反应的铁屑。
步骤3:滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL 水洗涤,分液得粗溴苯。
步骤4:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤即得粗产品。

(1)步骤1仪器a中发生的主要化学反应方程式为: 。
(2)仪器c的作用是冷凝回流,回流的主要物质有: 。
(3)步骤3中NaOH所发生的主要反应是: 。
(4)若将图1虚线框部分改为图2装置,则 D、E可以检验出来的物质是 ,其中试管C中苯的作用是 ,能否据此判断发生了取代反应? (填“是”或“否”)。
【答案】(1)![]() ;(2)苯、溴单质;
;(2)苯、溴单质;
(3)2NaOH+Br2=NaBr+NaBrO+H2O;(4)HBr,吸收溴蒸气,是。
【解析】
试题分析:(1)铁作催化剂苯与溴发生取代反应,反应方程式:![]() ;(2)根据上述资料得知,苯和液溴都是易挥发物质,苯和溴反应是放热反应,使部分苯和溴挥发,冷凝回流物质主要有苯、溴单质;(3)滤液中有溴苯和溶解在里面的溴单质,加入NaOH溶液,发生的反应的是:2NaOH+Br2=NaBr+NaBrO+H2O;(4)挥发出来的气体有溴蒸气、溴化氢气体,C中的苯作用除去挥发出来的溴蒸气(溴易溶于有机溶剂),D作用验证溴化氢,溴化氢使石蕊试液变红,E作用同样验证溴化氢,生成淡黄色沉淀,F作用除去多余的溴化氢,加成反应只能生成一种物质,故能判断发生的是取代反应。
;(2)根据上述资料得知,苯和液溴都是易挥发物质,苯和溴反应是放热反应,使部分苯和溴挥发,冷凝回流物质主要有苯、溴单质;(3)滤液中有溴苯和溶解在里面的溴单质,加入NaOH溶液,发生的反应的是:2NaOH+Br2=NaBr+NaBrO+H2O;(4)挥发出来的气体有溴蒸气、溴化氢气体,C中的苯作用除去挥发出来的溴蒸气(溴易溶于有机溶剂),D作用验证溴化氢,溴化氢使石蕊试液变红,E作用同样验证溴化氢,生成淡黄色沉淀,F作用除去多余的溴化氢,加成反应只能生成一种物质,故能判断发生的是取代反应。


 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】下表1是常温下几种弱酸的电离平衡上述(Ka)和弱碱的电离平衡常数(Kb),表2时常温下几种难(微)溶物的溶度积常数(Kap)
表1 | |
酸或碱 | 电离常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HIO3 | 1.7×10-1 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3H2O | 1.8×10-5 |
表2 | |
难(微)溶物 | 溶度积常数(Ksp) |
BaSO4 | 1×10-10 |
BaCO3 | 2.6×10-9 |
请回答下面问题:
(1)上述四种酸中,酸性最强的是______________(用化学式表示)。下列能使醋酸溶液中CH3COOH的电离度增大,而电离常数不变的操作是______(填序号)。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)HCOONH4的水溶液呈_______(选填“酸性”、“中性”、“碱性”),写出HCOONH4水解的离子反应方程式____________。
(3)物质的量1:1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为___。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,最终 SO42-物质的量浓度达到0.05mol·L-1,则此时溶液中CO32-物质的量浓度应_____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
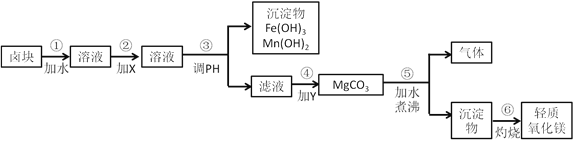
要求产品尽量不含杂质,而且生产成本较低,请根据表中提供的资料,回答下列问题。

(1)在步骤②中加入的试剂X,最佳的选择是______,其作用是__________;
(2)在步骤④中加入的试剂Y是_______________________;
(3)在步骤⑤中发生反应的化学方程式是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体0.1mol,完全燃烧得0.2molCO2和2.7gH2O,下列说法正确的是( )
A. 混合气体中一定有甲烷B. 混合气体可能是甲烷和乙烯
C. 混合气体中一定有乙烷D. 混合气体可能是乙烯和乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2可用作食品添加剂。NaNO2能发生以下反应:
3NO2-+2H+=NO3-+2NO↑+H2O NO2-+Ag+=AgNO2↓(淡黄色)
某化学兴趣小组进行以下探究。回答有关问题:
(l)制取NaNO2
反应原理:Na2CO3+2NO2=NaNO2+NaNO3+CO2
Na2CO3+NO+ NO2=2NaNO2+CO2
用下图所示装置进行实验。

① 铜与浓硝酸反应的化学方程式为___________。
② 实验过程中,需控制B中溶液的pH>7,否则产率会下降,理由是________。
③ 往C中通入空气的目的是_______________(用化学方程式表示)。
④ 反应结束后,B中溶液经蒸发浓缩、冷却结品、______等操作,可得到粗产品晶体和母液。
(2)测定粗产品中NaNO2的含量
称取mg粗产品,溶解后稀释至250mL。取出25.00 mL溶液,用cmol/LKMNO4酸性溶液平行滴定三次,平均消耗的体积为VmL。
已知:2MnO4-+6H++5NO2-=5NO3-+2Mn2++3H2O
① 稀释溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有______ (填标号)。
A.容量瓶 B.量筒 C.胶头滴管 D.锥形瓶
② 当观察到_______时,滴定达到终点。
③ 粗产品中NaNO2的质量分数为________(用代数式表示)。
(3)设计实验方案证明母液中含有NO2-_____________(限选用的试剂:硝酸、硝酸银溶液、硝酸钡溶液、氯化钡溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铜锌合金溶解后与足量KI溶液反应(Zn2+不与I-反应),生成的I2用Na2S2O3标准溶液滴定,根据消耗的Na2S2O3溶液体积可测算合金中铜的含量。实验过程如下图所示:

回答下列问题:
(1)H2O2的电子式为_________;“溶解”后铜元素的主要存在形式是______(填离子符号)。
(2)“煮沸”的目的是除去过量的H2O2。298K时,液态过氧化氢分解,每生成0.01molO2放出热量1.96kJ,该反应的热化学方程式为_______________。
(3)用缓冲溶液“调PH”是为了避免溶液的酸性太强,否则“滴定”时发生反应:
S2O32-+2H+=S↓+SO2↑+H2O
① 该缓冲溶液是浓度均为0.10mol/L的CH3COOH和CH3COONH4的混合溶液。25℃时,溶液中各种离子浓度由大到小的顺序为_________。
[已知:25℃时,Ka(CH3COOH)=Kb(NH3·H2O)=1.8×10-5]
② 若100 mL Na2S2O3溶液发生上述反应时,20s后生成的SO2比S多3.2g,则v(Na2S2O3)=_____mol/(L·s)(忽略溶液体积变化的影响)。
(4)“沉淀”步骤中有CuI沉淀产生,反应的离子方程式为_____________。
(5)“转化”步骤中,CuI转化为CuSCN,CuSCN吸附I2的倾向比CuI更小,使“滴定”误差减小。沉淀完全转化后,溶液中c(SCN -):c(I-)≥_______________。
[已知:Ksp(CuI)=1.1×10-12;Ksp(CuSCN)=4.4×10-15]
(6)下列情况可能造成测得的铜含量偏高的是______(填标号)。
A. 铜锌合金中含少量铁
B. “沉淀”时,I2与I-结合生成I3- :I2+I-=I3-
C. “转化”后的溶液在空气中放置太久,没有及时滴定
D. “滴定”过程中,往锥形瓶内加入少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应8NH3+3Cl2=N2+6NH4Cl,下列说法正确的是( )
A.N2是还原产物
B.Cl2是氧化剂
C.还原剂与氧化剂物质的量之比是3:2
D.还原产物与氧化产物物质的量之比是1 : 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A是制取溴苯的实验装置,B、C是改进后的装置。请仔细分析,对比三个装置,回答下列问题:


(1)写出三个装置中发生反应的主要化学方程式:________________。写出B中右边试管中所发生反应的化学方程式:__________________。
(2)装置A和C均采用了长玻璃导管,其作用是_______、____________。
(3)在实验B、C装好仪器及药品后要使反应开始,应对装置B进行的操作是________________;应对装置C进行的操作是_______________________。
(4)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是_________________。
(5)B中采用了洗气瓶吸收装置,其作用是______________________,反应后洗气瓶中可能出现的现象是_______________。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是_____________________;_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com