
【题目】化合物G是合成降压药替米沙坦的重要中间体,其人工合成路线如下:
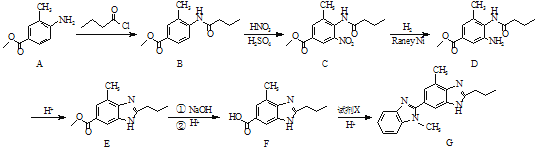
(1)C中含氧官能团的名称为酰胺键、_______和________。
(2)A→B的反应类型为______。
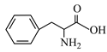
(3)试剂X的分子式为C7H10N2,写出X的结构简式:________。
(4)A的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______。
①是α-氨基酸;
②苯环上有3种不同化学环境的氢原子。
(5)已知:①苯胺(![]() )有还原性,易被氧化;
)有还原性,易被氧化;
②硝基苯直接硝化产物为间二硝基苯
③![]()
![]() CH3COO-+CH3NH2
CH3COO-+CH3NH2
写出以![]() 和
和![]() 为原料制备
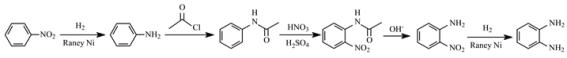
为原料制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________________________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________________________
【答案】酯基 硝基 取代反应 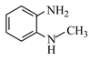
【解析】
A与![]() 发生取代反应生成B,B和浓硝酸在浓硫酸的作用下发生硝化反应生成C,C发生还原反应生成D,D在氢离子作用下生成E,E中酯基水解再酸化得到F,F与X反应生成G,该过程与D生成E的过程类似,X的分子式为C7H10N2,结合F和G的结构简式,可知X的结构简式为
发生取代反应生成B,B和浓硝酸在浓硫酸的作用下发生硝化反应生成C,C发生还原反应生成D,D在氢离子作用下生成E,E中酯基水解再酸化得到F,F与X反应生成G,该过程与D生成E的过程类似,X的分子式为C7H10N2,结合F和G的结构简式,可知X的结构简式为 。
。
(1)C中的含氧官能团为酰胺基、硝基、酯基;
(2)A生成B的过程中氨基上的氢原子被代替,属于取代反应;
(3)根据D转化为E的原理并结合F和G的结构可知,X为 ;
;
(4)A为 ,其同分异构体满足:
,其同分异构体满足:
①是α-氨基酸,即含有氨基和羧基,且氨基和羧基连接在同一个碳原子上;
②苯环上有3种不同化学环境的氢原子,则苯环上可能有一个取代基、三个不同的取代基或两个处于间位的相同取代基。综合两个条件可知,满足条件的结构为: ;
;
(5)对比![]() 和
和![]() 的结构可知需要在苯环上引入两个处于邻位的氨基,根据C到D变化可知硝基可以被还原为氨基,但硝基苯直接硝化产物为间二硝基苯,所以不能直接硝化硝基苯,再将硝基还原为氨基,根据A到D的过程可知
的结构可知需要在苯环上引入两个处于邻位的氨基,根据C到D变化可知硝基可以被还原为氨基,但硝基苯直接硝化产物为间二硝基苯,所以不能直接硝化硝基苯,再将硝基还原为氨基,根据A到D的过程可知![]() 可以和
可以和![]() 发生取代反应生成
发生取代反应生成 ,而且该物质取代基的邻位可以发生硝化反应,根据题干信息③可知该物质的取代基可以在碱性环境中生成氨基,综上所述,合成路线可以设计为:
,而且该物质取代基的邻位可以发生硝化反应,根据题干信息③可知该物质的取代基可以在碱性环境中生成氨基,综上所述,合成路线可以设计为: 。
。


科目:高中化学 来源: 题型:
【题目】为了验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹 持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.…
(1)A中反应的化学方程式为:KMnO4+HCl(浓)=KCl+MnCl2+Cl2↑+H2O,则氧化性KMnO4____Cl2(填“>”“<”或“=”)。
(2)验证氯气的氧化性强于碘的实验现象是____。
(3)过程Ⅲ的实验目的是____。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是____。
(5)浸有NaOH溶液的棉花团的作用是____。此处发生的化学方 程式是____。
(6)氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们单质氧化性强弱为:Cl2>Br2>(CN)2>(SCN)2>I2。试写出:在NaBr和KSCN的混合溶液中加入(CN)2的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全球气候变暖给人类的生存和发展带来了严峻的挑战,在此背景下,“新能源”、“低碳”、“节能减排”、“吃干榨尽”等概念愈来愈受到人们的重视。下列有关说法不正确的是
A. 太阳能、地热能、生物质能和核聚变能均属于“新能源”
B. “低碳”是指采用含碳量低的烃类作为燃料
C. 如图甲烷经一氯甲烷生成低碳烯烃的途径体现了“节能减排”思想

D. 让煤变成合成气,把煤“吃干榨尽”,实现了煤的清洁、高效利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 室温下,向苯酚钠溶液中通足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
B | 加热乙醇与浓硫酸的混合溶液,将产生的气体通入少量酸性KMnO4溶液,溶液紫红色褪去 | 有乙烯生成 |
C | 向5 mL 0.1 mol·L1 KI溶液中加入1 mL 0.1 mol·L1 FeCl3溶液,充分反应后,萃取分液,向水层中滴加KSCN溶液,溶液呈血红色 | I-与Fe3+的反应有一定限度 |
D | 向NaHCO3溶液中滴加紫色石蕊试液,溶液变蓝 | Kw<Ka1(H2CO3)×Ka2(H2CO3) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应:![]() 平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.30mol/L。下列有关判断正确的是
平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.30mol/L。下列有关判断正确的是
A.x+y﹤zB.平衡向正反应方向移动
C.B的转化率降低D.C的体积分数升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双缩脲反应可以用于测定蛋白质的含量。双缩脲反应的原理可表示如下:

双缩脲 紫红色配离子
(1)Cu2+的基态核外电子排布式为_______。
(2)与H2O互为等电子体的一种阳离子为_______(填化学式)。
(3)双缩脲分子中氮原子轨道的杂化类型是_______;1 mol双缩脲分子中含有σ键的数目为_______。
(4)该紫红色配离子中的配位原子为_______。
(5)Cu3Au的晶胞如下图所示,Cu3Au晶体中每个铜原子周围距离最近的铜原子数目为_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴是一种重要的化工材料,广泛应用于有机合成。一种以铜钴矿(主要成分为Co2CuS4,一定量CuFeS2)为原料,生产草酸钴晶体(CoC2O4·2H2O)的工艺流程:
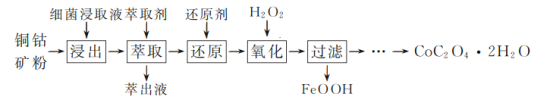
已知:①“浸出”液含有的离子主要有H+、Fe3+、Cu2+、Co3+、![]() ;
;
②pH增大,Fe2+被氧化的速率加快,同时生成的Fe3+水解形成更多的胶体;
③草酸钴晶体难溶于水;25℃时,Ksp[Co(OH)2]=1.6×10-15。
回答下列问题:
(1)生产时为提高铜钴矿粉浸出率,常采取的措施有________(填字母)。
a.适当延长浸出时间b.高温浸出c.分批加入细菌浸取液并搅拌
(2)“萃取”步骤中萃取除去的主要金属阳离子是________。
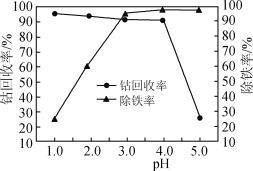
(3)“氧化”过程中,控制70℃、pH=4条件下进行,pH对除铁率和钴回收率的影响如图所示。
①用电子式表示H2O2的形成过程________。
②“氧化”过程的离子方程式为________。
③pH为4~5时,钴的回收率降低的原因是________。
(4)“过滤”后的滤液中加入(NH4)2C2O4溶液反应得到草酸钴晶体,过滤得到的草酸钴晶体需要用蒸馏水洗涤,检验晶体是否洗涤干净的方法是_______________。
(5)300℃时,在空气中煅烧CoC2O4·2H2O可制得Co3O4,该反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H 1=-90.7 kJ·mol-1 K1
CH3OH(g) △H 1=-90.7 kJ·mol-1 K1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1 K2
CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1 K2
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H 3=-41.2kJ·mol-1 K3
CO2(g)+H2(g) △H 3=-41.2kJ·mol-1 K3
回答下列问题:
(1)则反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的△H=____kJ·mol-1;该反应的平衡常数K=____(用K1、K2、K3表示)
CH3OCH3(g)+CO2(g)的△H=____kJ·mol-1;该反应的平衡常数K=____(用K1、K2、K3表示)
(2)下列措施中,能提高CH3OCH3产率的有____。
A.使用过量的CO B.升高温度 C.增大压强
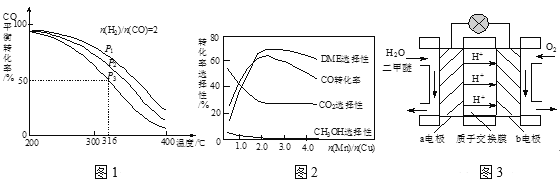
(3)将合成气以n(H2)/n(CO)=2通入1 L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图1所示,下列说法正确的是____。
CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图1所示,下列说法正确的是____。
A.△H <0
B.P1>P2>P3:
C.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%
(4)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚。观察图2回答问题。催化剂中n(Mn)/n(Cu)约为____时最有利于二甲醚的合成。
(5)图3为绿色电源“二甲醚燃料电池”的工作原理示意图,a电极的电极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在做原电池原理的实验时,有如下实验步骤:
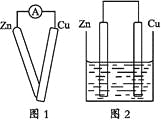
①用导线将灵敏电流计的两端分别与纯净的锌片和铜片相连接(如图1);
②把一块纯净的锌片插入盛有稀硫酸的烧杯中;
③把一块纯净的铜片插入盛有稀硫酸的烧杯中;
④用导线把锌片和铜片连接起来后,再平行地插入盛有稀硫酸的烧杯中(如图2)。
回答下列问题:
(1)实验步骤①中应观察到的现象是_______________________。
(2)实验步骤②中应观察到的现象是_______________________。
(3)实验步骤③中应观察到的现象是_______________________。
(4)实验步骤④中应观察到的现象是_______________________。
(5)通过实验步骤④该同学头脑中有了一个猜想(或假设),该猜想是_______。
(6)为了证实该猜想,该同学又设计了第⑤步实验,请简要画出第⑤步实验的装置示意图。______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com