
【题目】工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为![]() 计算:
计算:
(1)该条件下N2的平衡转化率;(小数点后保留一位)
(2)该条件下反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数。(不带单位)
N2(g)+3H2(g)的平衡常数。(不带单位)
【答案】(1)66.7%;(2)5.0×10-3
【解析】
试题分析:(1)设反应过程消耗x mol N2(g)。
N2(g) + 3H2(g)![]() 2NH3(g)
2NH3(g)
起始物质的量/mol 0.60 1.60 0
平衡物质的量/mol 0.60-x 1.60-3x 2x
平衡时反应体系总物质的量=mol=(2.20-2x)mol
NH3(g)的物质的量分数=2x÷(2.20-2x)=![]()
解得x=0.40mol
则N2的平衡转化率=![]() ×100%=66.7%。
×100%=66.7%。
(2)设反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数为K。
N2(g)+3H2(g)的平衡常数为K。
平衡时,c(NH3)=2×0.40 mol÷2.0 L=0.40 mol·L-1
c(N2)=(0.60-0.40)mol÷2.0 L=0.10 mol·L-1
c(H2)=(1.60-3×0.40)mol÷2.0 L=0.20 mol·L-1
K=![]() =
=![]() =5.0×10-3 。
=5.0×10-3 。


科目:高中化学 来源: 题型:
【题目】原电池是一种将____转变为____的装置。电子的流动方向是从电源的____极通过外电路流到电源的____极。电工操作中规定,不能把铜线和铝线拧在一起连接线路,这是因为在潮湿的空气中,铜与铝接触形成原电池,其中铝做____极,很快被腐蚀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年诺贝尔化学奖授予三位美国科学家,以表彰他们如光合作用叶绿体光反应时酶中、生物固氮时固氮酶中)的化学反应。
(1)固氮酶有铁蛋白和钒铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将环境底物乙炔催化还原成乙烯,下列说法正确的有________(不定项选择)。
a.每个C2H2和C2H4分子中的π键数目相同 b.碳负离子CH呈三角锥形
c. NO+电子式为 [∶NO∶]+ d.NH3沸点比N2高,主要是因为前者是极性分子
(2)钒可合成电池电极,也可人工合成二价钒(V)固氮酶(结构如图)
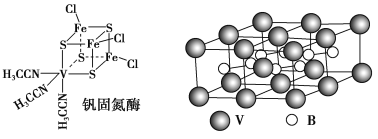
V元素位于周期表的______区,该原子基态时的价层电子排布式为___________________。
②钒固氮酶中钒的配位原子有________(写元素符号)。
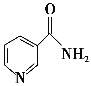
③熔融空气电池钒硼晶体晶胞结构如图所示,该晶胞中含有钒原子数目为________。
(3)烟酰胺(结构简式如图)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化轨道类型有 ,1 mol该分子中含σ键的数目为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修化学与技术】铝是一种重要的金属,在生产、生活中具有许多重要的用途,如下框图是从铝土矿中制备铝的工艺流程:

已知:①铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
②溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学方程式为:2Na2SiO3+2NaAlO2+4H2O=Na2Al2Si2O8↓+2H2O+4NaOH
回答下列问题:
(1)溶解铝土矿时,发生反应的离子方程式为:____________。
(2)滤渣A的主要成分________;硅铝酸盐沉淀写成氧化物的形式是________。
(3)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是 _。
(4)若该工厂用![]() kg铝土矿共制得
kg铝土矿共制得![]() kg Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为______。
kg Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为______。
(5)若将铝溶解,下列试剂中最好选用_____ __(填编号)。
A.浓硫酸B. 稀硫酸C.稀HNO3 D.浓HNO3
(6)电解冶炼铝时用Na3AlF6作助熔剂, Na3AlF6是配合物,其中内界是___,配位数为_ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体( Na2MoO4·2H2O)是一种无公害型冷却水系统的金属缓蚀剂。工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示:
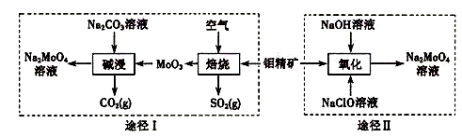
(1) NaClO的电子式是 。
(2)为了提高焙烧效率,除增大空气量外还可以采用的措施是 。
(3)途径I碱浸时发生反应的化学反应方程式为 。
(4)途径Ⅱ氧化时发生反应的离子方程式为 。
(5)分析纯的钼酸钠常用四钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与途径I所产生的尾气一起通入水中,得到正盐的化学式是 。
(6)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如下图:
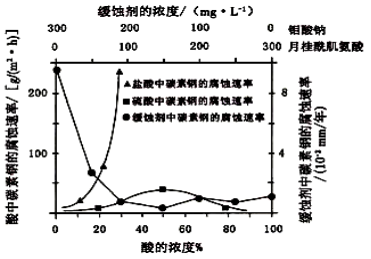
①要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为__ __。
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是 。
③试分析随着盐酸和硫酸浓度的增大,碳素钢在两者中腐蚀速率产生明显差异的主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用LiOH可制备锂离子电池正极材料。LiOH可由电解法制备,如右图,两极区电解质溶液分别为LiOH和LiCl溶液。下列说法错误的是
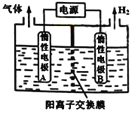
A.B极区电解质溶液为LiOH溶液
B.阳极电极反应式为2Cl--2e-=Cl2↑
C.电解过程中主要是H+通过阳离子交换膜向B电极迁移
D.电极A连接电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。请推断后回答下列问题:
(1)Z在Y单质中燃烧的产物电子式为
用电子式表示X与R化合物的形成过程
(2)Y、Z、W、R形成的简单离子半径由大到小顺序为
(3)W单质与Z的最高价氧化物对应的水化物反应的离子方程式为
W单质与R的最高价氧化物对应的水化物反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源、环境与人类的生活和社会发展密切相关。低碳、环保,能源的综合利用是是当今的热门话题。英国蒂斯河畔斯托克顿市的“空气燃料合成公司冶竟真的发明出了一种将空气变成汽油的高科技技术,而美国科学家最早设计出以甲烷等碳氢化合物为燃料的新型电池,大大提高天然气的利用效率。据此,回答下列问题:
(1)“空气变汽油”这项科技解决环境问题的意义是_______________________;
(2)“空气变汽油”其原理可简化如下:
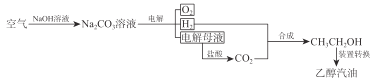
则:
①合成路线中,NaOH 和盐酸都可以循环利用,写出有关反应式______________________;
②转变过中,100g5%Na2CO3溶液,电解后,溶液浓度变为10%,则生成标准状况下的氢气多少升?
(3)天然气燃料电池最大的障碍是氧化反应不完全,产生________ (填写化学式)堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间。
(4)以下是天然气燃料电池电解精炼铜的装置图:
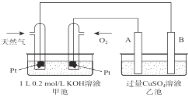
则,①甲池反应的离子方程式为______________________;
②当乙池中某电极的质量增重12.8g 时,理论上甲池中消耗的CH4在标准状况下的体积为__________mL,甲池中溶液的pH约为__________(溶液的体积变化忽略不计);此时向甲池中加入1 L1.0×10-3mol/L的CaCl2溶液,则甲池中________(填“有”或“无”)沉淀生成[已知Ksp(CaCO3)=2.9×10-9]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物K在化工和医药方面有重要的应用,其合成路线如下:

已知信息:
①C能发生银镜反应,E的相对分子质量比D大4,G的苯环上的一溴代物有两种
②![]()
![]()
![]()
③2RCH2CHO![]()
![]()
请回答下列问题:
(1)F的名称是__________,H含有的官能团是__________。
(2)A→B的反应类型是__________,F→G的反应类型是__________。
(3)C与银氨溶液反应的化学方程式是__________。
(4)K的结构简式是__________。
(5)符合下列要求的C8H10O的同分异构体有__________种.
①芳香族化合物②与Na反应并产生H2③遇FeCl3溶液呈紫色,
其中核磁共振氢谱为4组峰,且面积比为6:2:1:1的是__________(写出其中一种结构简式)
(6)参照已知信息和成路线,设计一条由CH2=CH2为原料合成CH3CH2CH2CH2OH的路线(注明反应条件):__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com