
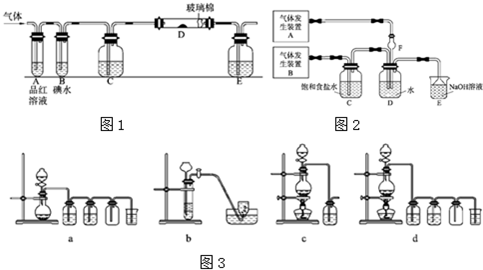
(12分)某兴趣小组研究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:

(1)SO2气体与Fe3+反应的主要产物是__ __ 。(填离子符号)
(2)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热浓H2SO4
(3)装置C的作用是 。
(4)如果有280mL SO2气体(已折算为标态)进入C装置中,则C中50mL NaOH溶液的物质的量浓度至少为 mol/L才能达到目的。
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 ,原因是 。
(6)能表明I—的还原性弱于SO2的现象是 ,写出有关离子方程式: 。
(1)SO42-、Fe2+(2分) (2)BD (2分)
(3)吸收多余的SO2,防止污染空气(1分), (4)0.25 (2分)
(5)方案①(1分)、SO2的水溶液也能使KMnO4溶液褪色(1分)
(6)B中蓝色溶液变无色(1分)、I2+SO2+2H2O=2I-+SO42-+4H+ (2分)
【解析】
试题分析:(1)SO2具有还原性,铁离子具有氧化性,二者发生氧化还原反应,即2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,所以SO2气体还原Fe3+反应的产物是Fe2+,SO42-。
(2)A、硝酸具有强氧化性,把亚硫酸钠氧化成硫酸钠,得不到二氧化硫,故A错;B、浓硫酸虽具有强氧化性,但不能氧化亚硫酸钠,能和亚硫酸钠反应生成SO2,故B正确;C、固体硫在纯氧中燃烧,操作不容易控制,故C错;D、铜与浓硫酸反应的离子方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,所以可以制备SO2,故D正确,因此选BD。
CuSO4+SO2↑+2H2O,所以可以制备SO2,故D正确,因此选BD。
(3)二氧化硫是酸性氧化物具有刺激性气味,属于大气污染物,直接排放污染大气,能和碱反应生成盐和水,所以可用碱液吸收二氧化硫,防止污染空气。
(4)280mL SO2气体(已折算为标态)物质的量=0.28L÷22.4L/mol=0.0125mol,SO2是酸性氧化物,进入C装置中发生反应为SO2+NaOH=NaHSO3,则C中消耗氢氧化钠物质的量为0.0125mol,50mL NaOH溶液的浓度至少=0.0125mol÷0.05L=0.25mol/L。
(5)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,而Fe2+也使高锰酸钾溶液褪色,因此方案①不合理。
(6)二氧化硫能使含有碘的淀粉溶液褪色,说明发生了氧化还原反应,碘是氧化剂,二氧化硫是还原剂,还原剂的还原性大于还原产物的还原性,据此能表明I—的还原性弱于SO2的还原性,反应的离子方程式为I2+SO2+2H2O=2HI+H2SO4。
考点:考查SO2制备以及性质的实验探究、实验方案设计与评价、氧化还原反应的应用等


科目:高中化学 来源: 题型:阅读理解
| 催化剂 |
| 加热 |
| C7(N2)C12(H2O) |
| C6(NO2)C8(NH3) |
| C7(N2)C12(H2O) |
| C6(NO2)C8(NH3) |
| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| 0.2 |
| t1 |
| 0.2 |
| t1 |
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市五区县高三质量检查试卷(一)理综化学试卷(解析版) 题型:实验题
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源。
(1)某兴趣小组采用如图所示装置制取SO2

①下列实验方案适用如图所示装置制取所需SO2的试剂是_______(填序号)。
A.Na2SO3溶液与稀硝酸
B.Na2SO3固体与浓硫酸
C.固体硫和氧气
D.铜与浓硫酸
②a的仪器名称是_______。
③尾气吸收装置的连接顺序是b接( )接 ( )接e。
(2)为了回收利用SO2废气,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体( 生产流程,其流程示意图如下:
生产流程,其流程示意图如下:

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时溶液的pH见下表:

请回答:
①含Al3+的盐常用作净水剂,用离子方程式表示其净水原理________________________。
②浸出过程中主要反应的化学方程式是___________________________________________。
③氧化过程中加入MnO2粉的目的是______________________________________________;
反应的离子方程式是_________________________________________________________。
④用石灰浆调节pH,pH应调节的范围是___________________________________。
⑤滤渣的主要成分是____________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江西省南昌市高三第三次模拟考试理综化学试卷(解析版) 题型:实验题
某兴趣小组研究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:

(1)SO2气体与Fe3+反应的主要产物是____、 。(填离子符号)
(2)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热浓H2SO4
(3)装置C的作用是 。
(4)如果有280mL SO2气体(已折算为标态)进入C装置中,则C中,50mL NaOH溶液的浓度至少为 mol/L才能达到目的。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 ,原因是 。
(6)能表明I—的还原性弱于SO2的现象是 ,写出有关离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com