
当温度为70℃时,Cl2与NaOH溶液能同时发生两个自身氧化还原反应:①Cl2+2NaOH== NaCl+NaClO+H2O;②3Cl2+6NaOH==5NaCl+NaClO3+3H2O。若反应完全后测得溶液中NaClO和NaClO3的物质的量之比为4:1,则溶液中NaCl和NaClO的物质的量浓度之比为 ( )
A.11:2 B.9:4 C.1:1 D.5:1
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率 (×10-3mol?L-1?min-1) |
7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
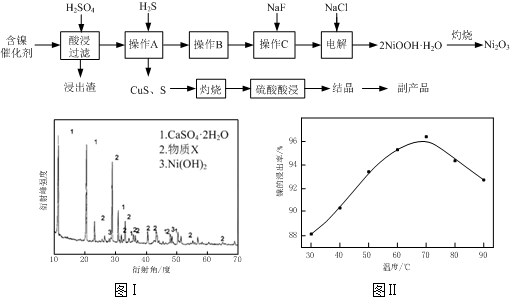
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.11∶2 B.9∶4 C.1∶1 D.5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
A.11∶2 B.9∶4 C.1∶1 D.5∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com