
【题目】下列说法正确的是 ( )
A.石油的分馏、煤的干馏都是物理变化
B.化学反应的限度是不可改变的
C.可用乙醇萃取溴水中的溴
D.在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子组在指定溶液中一定能大量共存的是( )
A.使pH试纸呈蓝色的溶液中:I-、Cl-、NO3-、Cu2+
B.使酚酞呈深红色的溶液中:Na+、Cl- 、H+、NO3-
C.含大量Ag+ 的溶液中:K+、Na+、NO3-、SO42-
D.含大量OH- 的溶液中:CO32-、Cl-、F- 、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s)═CuSO4(s)+5H2O(l)△H=+Q2kJmol-1则Q1、Q2的关系为
A. Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种短周期元素的原子半径及主要化合价如下表:
元素符号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是( )
A.X、Y元素的金属性X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.一定条件下,W单质可以将Z单质从其氢化物中置换出来
D.Y的最高价氧化物对应的水化物能溶于稀氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A.H2O2的电子式:![]()
B.铝离子的结构示意图:![]()
C.质子数为35、中子数为45的溴原子:![]() Br
Br
D.![]() C与
C与![]() C互为同素异形体
C互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性
Ⅰ.实验室制备FeBr2
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管.e是两只耐高温的瓷皿,其中盛有细铁粉.
实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,不断将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁
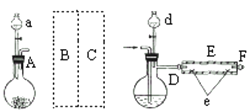
请回答:
(1)如何检查用塞子(插有导管和仪器)塞紧的D的气密性________.
(2)若在A中盛固体CaCO3,a中盛6mol/L盐酸,为使导入D中的CO2为干燥纯净的气体,则图中B、C处的装置和其中的试剂应是:B为________,C为________.为防止污染空气,实验时应在F处连接盛________的尾气吸收装置
(3)反应过程中要不断通入CO2,其主要作用是①________,②________.
Ⅱ.探究FeBr2的还原性,
(1)实验需要90 mL 0.1 mol·L-1FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外还需的玻璃仪器是________。
(2)取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。
设计实验证明假设2是正确的_______________________________
(3)实验证明:还原性Fe2+>Br-请用一个离子方程式来证明:______________________________;
(4)若在40mL上述FeBr2溶液中通入3×10-3molCl2,则反应的离子方程式为:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应2N2O5(g)═4NO2(g)+O2(g)开始时,c(N2O5)=0.040 8molL﹣1,经1min后,c(N2O5)=0.030 0molL﹣1.则该反应的反应速率为( )
A.v(N2O5)=1.80×10﹣3 molL﹣1min﹣1
B.v(N2O5)=1.08×10﹣2 molL﹣1min﹣1
C.v(NO2)=1.80×10﹣3 molL﹣1min﹣1
D.v(O2)=1.80×10﹣2 molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:制备溴乙烷的的一种方法是乙醇与氢溴酸反应,该反应的化学方程式为:CH3CH2OH+HBr![]() CH3CH2Br+H2O。
CH3CH2Br+H2O。
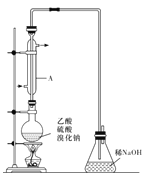
I.实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是 。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 (填写正确选项的字母)。
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
II.溴乙烷的性质实验
(4)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是 。通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液
(5)溴乙烷与NaOH乙醇溶液共热可产生乙烯气体。在进行该实验时,把生成的气体通过右图所示的装置。用该装置进行实验的目的是检验乙烯的生成,该图中右侧试管中的现象是______________;左侧试管中水的作用是___________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com