
ijĪĀ¶ČŹ±£¬°Ń1molN2O4ĘųĢåĶØČėĢå»żĪŖ10LµÄÕęæÕČŻĘ÷£¬Į¢¼“³öĻÖŗģ×ŲÉ«£¬·“Ó¦½ųŠŠ4sŹ±£¬NO2µÄÅضČĪŖ0£®04mol/L£¬ŌŁ¾¹żŅ»¶ĪŹ±¼äŗ󣬷“Ó¦“ļĘ½ŗā£¬ÕāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1£®8±¶£®ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
A£®Ē°4sÖŠŅŌN2O4µÄÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0£®01mol/L”¤s
B£®ŌŚ4sŹ±ČŻĘ÷ÄŚµÄŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1£®2±¶
C£®ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚŗ¬N2O40£®4mol
D£®ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚŗ¬NO21£®6mol
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ»īĢāĒɽāĒÉĮ·”¤øßæ¼»Æѧ£ØµŚŅ»ĀÖ£© ĢāŠĶ£ŗ022
ijĪĀ¶ČŹ±£¬°Ń1molĘųĢåA2(µ„ÖŹ)Óė1molĘųĢåB2(µ„ÖŹ)·ÅČėČŻ»żĪŖ1LµÄĆܱÕČŻĘ÷ÖŠ£¬Ź¹Ę䷓Ӧɜ³ÉĘųĢåC£¬2minŗó²āµĆČŻĘ÷ÖŠc(A2)£½0.4mol/L£¬c(B2)£½0.8mol/L£¬c(C)£½0.4mol/L£¬Ōņ“Ė·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ(CµÄ×é³É±ŲŠėÓĆA£¬B±ķŹ¾)________£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2010ÄźĮÉÄžŹ”¶«±±Óż²ÅѧŠ£øßŅ»ĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌĢā ĢāŠĶ£ŗĢīæÕĢā
£Ø10·Ö£©Ä³ĪĀ¶ČŹ±£¬°Ń1mol/LN2O4ĘųĢåĶØČėĢå»żĪŖ10LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ£¬Į¢¼“³öĻÖ×ŲÉ«£¬·“Ó¦½ųŠŠ4sŹ±NO2µÄÅضČĪŖ0.04mol/L£¬ŌŁ¾¹żŅ»¶ØŹ±¼äŗ󣬷“Ó¦µ½“ļĘ½ŗā£¬ÕāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1.8±¶”£
£Ø1£©Ē°4sÖŠŅŌN2O4µÄÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁ¶ČĪŖ mol/L”¤s”£
£Ø2£©ŌŚ4sŹ±ČŻĘ÷ÄŚµÄŃ¹ĒæĪŖæŖŹ¼Ź±µÄ ±¶”£
£Ø3£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚŗ¬N2O4 mol”£
£Ø4£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚNO2µÄÅضČĪŖ mol/L”£
£Ø5£©N2O4µÄ×Ŗ»ÆĀŹĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013ѧğĮÉÄžŹ”¶«±±Óż²ÅĖ«ÓļѧŠ£øßŅ»ĻĀѧʌʌ֊æ¼ĪÄæĘ»Æѧ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢīæÕĢā
ŅŃÖŖNO2ŗĶN2O4æÉŅŌĻą»„×Ŗ»Æ£ŗ N2O4 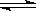 2NO2£¬Ä³ĪĀ¶ČŹ±£¬°Ń1mol N2O4ĘųĢåĶØČėĢå»żĪŖ10LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ£¬Į¢¼“³öĻÖ×ŲÉ«£¬·“Ó¦½ųŠŠ4sŹ±NO2µÄÅضČĪŖ0.04mol/L£¬ŌŁ¾¹żŅ»¶ØŹ±¼äŗ󣬷“Ó¦µ½“ļĘ½ŗā£¬ÕāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1.8±¶”£
2NO2£¬Ä³ĪĀ¶ČŹ±£¬°Ń1mol N2O4ĘųĢåĶØČėĢå»żĪŖ10LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ£¬Į¢¼“³öĻÖ×ŲÉ«£¬·“Ó¦½ųŠŠ4sŹ±NO2µÄÅضČĪŖ0.04mol/L£¬ŌŁ¾¹żŅ»¶ØŹ±¼äŗ󣬷“Ó¦µ½“ļĘ½ŗā£¬ÕāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1.8±¶”£
£Ø1£©Ē°4sÖŠŅŌN2O4µÄÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁ¶ČĪŖ mol/L”¤s
£Ø2£©ŌŚ4sŹ±ČŻĘ÷ÄŚµÄŃ¹ĒæĪŖæŖŹ¼Ź±µÄ ±¶
£Ø3£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚŗ¬N2O4 mol
£Ø4£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚNO2µÄÅضČĪŖ mol/L
£Ø5£©Ę½ŗāŹ±N2O4µÄ×Ŗ»ÆĀŹĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĮÉÄžŹ”¶«±±Óż²ÅĖ«ÓļѧŠ£øßŅ»ĻĀѧʌʌ֊æ¼ĪÄæĘ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŅŃÖŖNO2ŗĶN2O4æÉŅŌĻą»„×Ŗ»Æ£ŗ N2O4 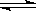 2NO2£¬Ä³ĪĀ¶ČŹ±£¬°Ń1mol
N2O4ĘųĢåĶØČėĢå»żĪŖ10LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ£¬Į¢¼“³öĻÖ×ŲÉ«£¬·“Ó¦½ųŠŠ4sŹ±NO2µÄÅضČĪŖ0.04mol/L£¬ŌŁ¾¹żŅ»¶ØŹ±¼äŗ󣬷“Ó¦µ½“ļĘ½ŗā£¬ÕāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1.8±¶”£
2NO2£¬Ä³ĪĀ¶ČŹ±£¬°Ń1mol
N2O4ĘųĢåĶØČėĢå»żĪŖ10LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ£¬Į¢¼“³öĻÖ×ŲÉ«£¬·“Ó¦½ųŠŠ4sŹ±NO2µÄÅضČĪŖ0.04mol/L£¬ŌŁ¾¹żŅ»¶ØŹ±¼äŗ󣬷“Ó¦µ½“ļĘ½ŗā£¬ÕāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1.8±¶”£
£Ø1£©Ē°4sÖŠŅŌN2O4µÄÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁ¶ČĪŖ mol/L”¤s
£Ø2£©ŌŚ4sŹ±ČŻĘ÷ÄŚµÄŃ¹ĒæĪŖæŖŹ¼Ź±µÄ ±¶
£Ø3£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚŗ¬N2O4 mol
£Ø4£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚNO2µÄÅضČĪŖ mol/L
£Ø5£©Ę½ŗāŹ±N2O4µÄ×Ŗ»ÆĀŹĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĪĀ¶ČŹ±£¬°Ń1mol/LN2O4ĘųĢåĶØČėĢå»żĪŖ10LµÄÕęæÕĆܱÕČŻĘ÷ÖŠ£¬Į¢¼“³öĻÖ×ŲÉ«£¬·“Ó¦½ųŠŠ4sŹ±NO2µÄÅضČĪŖ0.04mol/L£¬ŌŁ¾¹żŅ»¶ØŹ±¼äŗ󣬷“Ó¦µ½“ļĘ½ŗā£¬ÕāŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1.8±¶”£
£Ø1£©Ē°4sÖŠŅŌN2O4µÄÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁ¶ČĪŖ mol/L”¤s”£
£Ø2£©ŌŚ4sŹ±ČŻĘ÷ÄŚµÄŃ¹ĒæĪŖæŖŹ¼Ź±µÄ ±¶”£
£Ø3£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚŗ¬N2O4 mol”£
£Ø4£©ŌŚĘ½ŗāŹ±ČŻĘ÷ÄŚNO2µÄÅضČĪŖ mol/L”£
£Ø5£©N2O4µÄ×Ŗ»ÆĀŹĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com