
Ϊ�˼���ij���������Ƿ���![]() ��
��![]() ��Fe2+�ͽᾧˮ����������в������裺��ȡ�����û�������ȣ������Թܿڴ���Һ�壬��Һ����ʹ��ˮ����ͭ����������ȡ�����û���������ˮ�У��μ���������ˮ���ټ���KSCN��Һ����Ѫ��ɫ���֣���ȡ������Һ���Թ��У��������ᣬû�������ټ���BaCl2��Һ���а�ɫ�������ɣ���ȡ������Һ���Թ��У�����Ũ��NaOH��Һ������ʹʪ��ĺ�ɫʯ����ֽ���������������ͬʱҲ�а�ɫ�����������ó����ܿ��ɻ���ɫ������
��Fe2+�ͽᾧˮ����������в������裺��ȡ�����û�������ȣ������Թܿڴ���Һ�壬��Һ����ʹ��ˮ����ͭ����������ȡ�����û���������ˮ�У��μ���������ˮ���ټ���KSCN��Һ����Ѫ��ɫ���֣���ȡ������Һ���Թ��У��������ᣬû�������ټ���BaCl2��Һ���а�ɫ�������ɣ���ȡ������Һ���Թ��У�����Ũ��NaOH��Һ������ʹʪ��ĺ�ɫʯ����ֽ���������������ͬʱҲ�а�ɫ�����������ó����ܿ��ɻ���ɫ������
����˵����ȷ���У� ��
A.���е�����˵��һ����Fe2+
B.Ϊ�˼���![]() �����Խ����е��Լ���ΪHNO3�ữ��Ba(NO3)2
�����Խ����е��Լ���ΪHNO3�ữ��Ba(NO3)2
C.ͨ������ʵ���ȷ���û�����Ļ�ѧʽΪ��NH4��2Fe(SO4)2��6H2O
D.���еij�����ʱ����û��ɺ��ɫ����
D
���е�����ֻ��˵���û����ﺬ�нᾧˮ�����е�������ֻ��˵���û������к���Fe2+��Fe3+�����е�����˵���û�������һ������![]() �������HNO3�ữ��Ba(NO3)2,��
�������HNO3�ữ��Ba(NO3)2,��![]() Ҳ�������������˵���û������к�
Ҳ�������������˵���û������к�![]() �����е�����˵���û������к�Fe2+��
�����е�����˵���û������к�Fe2+��![]() ������ӦΪFe(OH)2,Fe(OH)2���ױ������е�O2�����ɺ��ɫ����Fe(OH)3��ͨ����������ֻ��ȷ���û������к�Fe2+��
������ӦΪFe(OH)2,Fe(OH)2���ױ������е�O2�����ɺ��ɫ����Fe(OH)3��ͨ����������ֻ��ȷ���û������к�Fe2+��![]() ��
��![]() �ͽᾧˮ������ȷ���仯ѧʽ����ֻ��D��ȷ��
�ͽᾧˮ������ȷ���仯ѧʽ����ֻ��D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

- 4 |
| 1000.00 mL |
| 20.00 mL |
| 10 g��20.00%-1.68 g |
| 10 g��20.00% |
| 1000.00 mL |
| 20.00 mL |
| 10 g��20.00%-1.68 g |
| 10 g��20.00% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
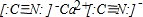
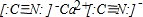
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�˼���ij���������Ƿ���NH4+��SO42-��Fe2+�ͽᾧˮ����������в������裺
��ȡ����������ȣ������Թܿڴ���Һ�壬�Ҹ�Һ����ʹ��ˮ����ͭ������
����ȡ������������ˮ�У�����KSCN��Һ���ٵμ���������ˮ���к�ɫ���֣�
��ȡ������Һ���Թܣ��������ᣬû�з�Ӧ�����ټ���BaC12��Һ���а�ɫ�������ɣ� ��ȡ������Һ���Թ��У�����ŨNaOH��Һ������ʹʪ��ĺ�ɫʯ����ֽ���������������ͬʱҲ�а�ɫ�����������ó����ܿ��ɻ���ɫ������
����˵������ȷ���� �� ��
A�����е�����˵����Fe2+
B��ͨ������ʵ���ȷ���û�����Ļ�ѧʽΪ��NH4��2Fe��SO4��2?6H2O
C��Ϊ�˼��SO2-4�����Խ����е��Լ���ΪHNO3�ữ��Ba��NO3��2
D�����еij�����ʱ����û����ɫ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com