
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
硫酸是中学化学实验室的常见药品,其性质有①酸性 ②吸水性 ③脱水性 ④强氧化性 ⑤催化作用,请将序号填在相应的横线上:
(1)锌和稀H2SO4制H2________;
(2)浓硫酸作干燥剂________;
(3)浓硫酸与蔗糖的炭化实验(黑面包实验)________;
(4)实验室用乙醇和冰醋酸制取乙酸乙酯________;
(5)乙酸乙酯的水解________;
(6)纤维素的水解________;
(7)浓硫酸与铜的反应________;
(8)浓硫酸使湿润石蕊试纸变红,后来又变黑________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为Na2S的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是ρ g·cm-3,试计算Na+与S2-的最短距离________(阿伏加德罗常数用NA表示 ,只写出计算式)。
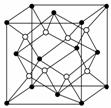
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分子晶体中,关于熔、沸点高低的叙述中,正确的是( )
A.Cl2>I2
B.SiCl4<CCl4
C.NH3>PH3
D.C(CH3)4>CH3CH2CH2CH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
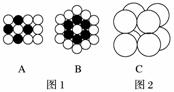
(1)将等径圆球在二维空间里进行排列,可形成密置层和非密置层。在图1所示的半径相等的圆球的排列中,A属于________层,配位数是________;B属于________层,配位数是________。
(2)将非密置层一层一层地在三维空间里堆积,得到如图2所示的一种金属晶体的晶胞,它被称为简单立方堆积,在这种晶体中,金属原子的配位数是______,平均每个晶胞所占有的原子数目是__________。
(3)有资料表明,只有钋的晶体中的原子具有如图2所示的堆积方式。钋位于元素周期表的第__________周期第________族,元素符号是________,最外层电子排布式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
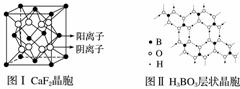
下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:
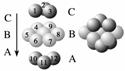
图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为________________________________________________________________________。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3 晶体中B原子个数与极性键个数比为____________。
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用________理论。
(4)三种晶体中熔点最低的是________(填化学式),其晶体受热熔化时,克服的微粒之间的相互作用为________________________________________________________________________
________________________________________________________________________。
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与有机物的结构、性质有关的叙述正确的是( )
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.医用酒精的浓度通常为95%
C.乙醇可以被氧化为乙酸,二者都能发生取代反应
D.淀粉和蛋白质均可作为生产葡萄糖的原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com