
【题目】下列只含有共价键的化合物是( )
A.Cl2B.IClC.NaOHD.NH4H
科目:高中化学 来源: 题型:
【题目】利用工业冶炼硫酸铜(含有Fe2+、AsO2-、Ca2+等杂质)提纯制备电镀硫酸铜的生产流程如下:

已知:①Fe3+、Cu2+开始沉淀的pH分别2.7、5.4,完全沉淀的pH分别为3.7、6.4。
②Ksp[Cu(OH)2]=2×10-20
③AsO2-+H2O2+H+=H3AsO4, H3AsO4+Fe3+=FeAsO4↓+3H+
(1)溶解操作中需要配制含铜32 g·L-1的硫酸铜溶液1.0 L,需要称量冶炼级硫酸铜的质量至少为___________g。
(2)测定溶解液中的Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4溶液应使用
________(“酸式”或“碱式”)滴定管,其中反应离子方程式为:______________________。若要检验调节pH后溶液中的Fe3+已除尽的方法是___________________________。
(3)氧化后需要将溶液进行稀释及调节溶液的pH=5,则稀释后的溶液中铜离子浓度最大不能超过____________mol·L-1。
(4)固体Ⅰ的主要成分除 FeAsO4 、Fe(OH)3外还有__________________,由溶液Ⅰ获得CuSO4·H2O,需要经过________ 、____________、过滤、洗涤、干燥操作。
(5)利用以上电镀级硫酸铜作为电解质溶液,电解粗铜(含锌、银、铂杂质)制备纯铜,写出阳极发生的电极反应式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息回答问题
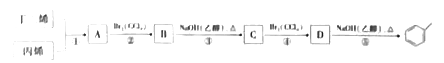
已知:![]()
(1)A中含有的官能团名称是______,A的名称是_____。
(2)不考虑顺反异构,丙烯的二氯代物有____种。
(3)反应类型:①是_________;⑤是_______________。
(4)反应③的化学方程式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取92g乙醇和60g乙酸反应,如果实际产率是理论产率的67%,则可得到乙酸乙脂的质量近似为是( )
A. 59g B. 88g C. 149.6g D. 176g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、M、N 的原子序数依次增大,且原子最外层电子数之和为23。X 的原子半径比Y 的小,X 与W 同主族,Z 的最外层电子数是电子层数的3倍,M 是地壳中含量最高的金属元素。
(1)M的离子结构示意图____________;X、Y形成的含18电子的化合物的电子式____________;
用电子式表示由W、Z形成的只含离子键的化合物的形成过程______________________;
(2)Y、Z、M原子半径由大到小的顺序____________(用元素符号表示),Z的氢化物稳定性_____N的氢化物稳定性(填“>” “<”或 “=”)
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是_________(填化学式),此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨气,相应的离子方程式为:___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应,其产物的颜色按红、淡黄、蓝色、浅绿色顺序排列的是( ) ①金属钠在纯氧中燃烧 ②铁与足量的稀硫酸反应 ③FeCl3溶液中滴入KSCN溶液④无水硫酸铜放入医用酒精中.
A.②③①④
B.③②①④
C.③①②④
D.③①④②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素 W、X、Y、Z,原子序数依次增大,请回答下列问题。
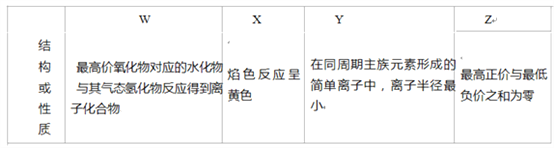
(1)Z 在元素周期表中位于_____族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学 反应,该元素是_____(填元素符号).
(3)① 下列可作为比较 X 和 Y 金属性强弱的依据是_____(填序号).
a.自然界中的含量 b.单质与酸反应时失去的电子数
c.单质与水反应的难易程度 d.最高价氧化物对应水化物的碱性
② 从原子结构的角度解释 X 的金属性强于 Y 的原因:_____,原子半径 X>Y,所以原子核 对最外层电子的吸引力 X失电子能力 X>Y.
(4)W 的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与 X 的最高 价氧化物对应的水化物混合,反应的化学方程式是_____。
(5)Y 单质和 Mg 组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。

能确定混合物中 Y 的质量分数的数据有_____(填序号).
a. m、n b. m、y c. n、y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
工业上以Ni的氧化物作催化剂,将丙烯胺氧化制得丙烯腈(CH2=CHCN),然后以H3PO4-K3PO4等作为电解质溶液,控制pH在8 5-9 0范围内,电解丙烯腈制己二腈、电解的总化学方程式为:4CH2=CHCN +2H2O![]() O2↑+2NC(CH2)4CN
O2↑+2NC(CH2)4CN
(1)Ni原子的核外电子排布式为____________________;在电解的总化学方程式所涉及的元素中,电负性由小到大的顺序为_________________________。
(2)PO43-的空间构型是_____________,CH2=CHCN中碳原子的杂化方式为__________________。
(3)NC(CH2)4CN分子中σ键与π键数目之比为_________________________。
(4)已知K3PO4是离子晶体,写出其主要物理性质______________(写出2条即可)。
(5)该电解总化学方程式中各元素组成的下列物质中,存在分子内氢健的是_________(填标号)。
A.NH3 B.H2O2 C. 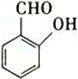 D.
D. 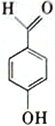
(6)金刚石的晶胞结构如右图。该晶胞中C原子数为_____________,若金刚石晶胞的密度是d g·cm-3,阿伏加德罗常数为NA,则金刚石晶胞中两个碳原子之间的最短距离为_____________。(用含d、NA的式子表示,只需要列出表达式即可)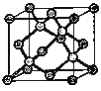
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com