
| m |
| M |
| n |
| V |
| V |
| Vm |
| n |
| V |
| m |
| M |
| 1 |
| 2 |
| 1000g |
| 18g/mol |
| 55.5mol |
| 1L |
| 0.25L |
| 22.4L/mol |
| 0.011mol |
| 1L |
| 90g |
| 18g/mol |
| 5mol |
| 100 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:阅读理解
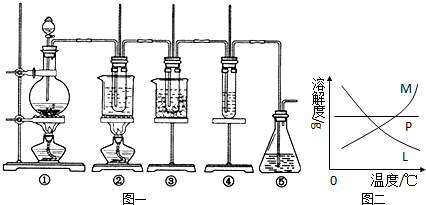
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
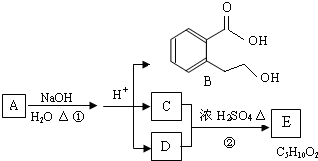
| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |


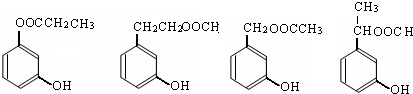 写出四者之一即可
写出四者之一即可 写出四者之一即可
写出四者之一即可| 实验编号 | C物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液的pH |
| m | 0.1 | 0.1 | pH=9 |
| n | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/mL HCl的质量分数:36.5%(1)该浓盐酸中HCl的物质的量浓度为 11.9mol/L 11.9mol/L .(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 BD BD (填编号).A.溶液中HCl的物质的量B.溶液的浓度C.溶液中Cl-的数目D.溶液的密度 (3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸.该该学生需要量取 16.8 16.8 mL(小数点后保留一位)上述浓盐酸进行配制.②现有a.10mL量筒;b.25mL量筒;c.烧杯;d.托盘天平.e.500mL容量瓶;f.胶头滴管;g.玻璃棒,请从其中选取必要的仪器,按各仪器第一次使用先后顺序排序: bcgef或bfcge bcgef或bfcge (填编号).③在配制过程中,下列实验操作对所配制盐酸物质的量浓度有何影响?(在空格中填“偏高”、“偏低”或“无影响”):定容时俯视观察 偏高 偏高 ;定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水偏低 偏低 .
查看答案和解析>> 科目:高中化学 来源: 题型: 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置先进行了有关实验: 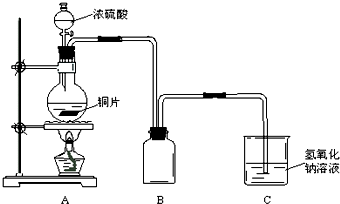 (1)B是用来收集实验中产生的气体的装置,但未将导管画全,请直接在原图上把导管补充完整. (2)实验中他们取6.4g铜片和12mL 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余. ①请写出铜跟浓硫酸反应的化学方程式: ②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是: (3)为定量测定余酸的物质的量浓度,某位同学进行了如下设计: 先测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度.他认为测定SO2的量的方法有多种,请问下列实验方案中不可行的是 A.将装置A产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量 B.将装置A产生的气体缓缓通入足量NaOH溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀 C.用排水法测定装置A产生气体的体积. 查看答案和解析>> 科目:高中化学 来源:同步题 题型:填空题 (1)某温度下纯水的c(H+)=2.0×10-7mol/L。在此温度下,某溶液中由水电离出的c(H+)为4.0× 10-13 mol/L,则该溶液的pH可能是____。 (2)分别将少量CO2气体通入一元酸的钠盐NaA和NaB的溶液中,发生的反应为: ①CO2+2NaA+ H2O==Na2CO3+2HA; ②CO2+NaB+H2O==NaHCO3+HB, 试由此推断H2CO3、HCO3-、HA、HB 的电离程度由大到小顺序为___。 (3)已知在相同条件下,HCN的电离程度比HF小。请根据有关知识分析判断,在相同温度下,物质的量浓 度相同的NaCN溶液和NaF溶液中: [c(CN-)+c(OH-)]____[f(F-)+c(OH-)] (选填“等于”、“大于”或“小于”)。 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |