
 |  |  | 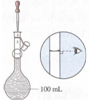 |
| A.接近称量质量时,轻振手腕,加够药品 | B.溶解时,用量筒控制所加蒸馏水的量 | C.移液时,玻璃棒插在刻度线以上,防止液体洒出 | D.接近刻度线1~2 cm时,用胶头滴管滴加蒸馏水至刻度线 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.称量固体时,当接近称量质量时,应用左手拿药匙,右手轻轻振动左手手腕;
B.为防止溶解和洗涤时所用蒸馏水的体积超过容量瓶容积,溶解时应用量筒控制所加蒸馏水的量;
C.移液时,玻璃棒应插在刻度线以下;
D.依据定容时正确操作解答.
解答 解:A.称量固体时,当接近称量质量时,应用左手拿药匙,右手轻轻振动左手手腕,加够药品,图示操作正确,故A不选;
B.为防止溶解和洗涤时所用蒸馏水的体积超过容量瓶容积,溶解时应用量筒控制所加蒸馏水的量,图示操作正确,故B不选;
C.图示移液操作中,玻璃棒插在刻度线以上,应插在刻度线以下,故C选;
D.定容时,当液面接近刻度线1~2 cm时,用胶头滴管滴加蒸馏水至刻度线,图示正确,故D不选;
故选:C.
点评 本题考查了化学实验的基本操作,明确一定物质的量浓度溶液配制原理及正确的操作步骤是解题关键,注意容量瓶使用方法和注意问题,题目难度不大.


科目:高中化学 来源: 题型:解答题

 由C→D的反应类型是取代反应
由C→D的反应类型是取代反应
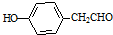
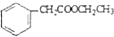 的合成路线流程图(无机试剂可任选).合成路线流程图示例如图:H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH
的合成路线流程图(无机试剂可任选).合成路线流程图示例如图:H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH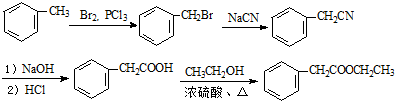 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子符号 | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 2.5 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X原子的最外层只有1个电子 | |
| B. | 元素X常见化合价为+3 | |
| C. | X原子核外有3个未成对电子 | |
| D. | 元素X最高价氧化物的水合物为强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 粉末中一定有Na2O、Na202、NaHC03 | |
| B. | 粉末中一定不含有Na2C03和NaCl | |
| C. | 粉末中一定不含有Na20和NaCl | |
| D. | 无法肯定粉末里是否含有NaHCO3和NaC1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 把铜片和铁片放在盛有稀食盐水和酚酞混合液的U形管中,如图所示,最终可在A极观察到酚酞变红.填空完成问题:
把铜片和铁片放在盛有稀食盐水和酚酞混合液的U形管中,如图所示,最终可在A极观察到酚酞变红.填空完成问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
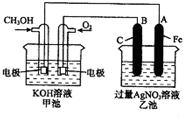 如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com