
在一固定容积的密闭容器中充入2mol NO2,一定温度下建立如下平衡:2 NO2(g) N2O4(g),此时平衡混合气体中NO2的体积分数为x%;若再充入1mol N2O4,在温度不变的情况下, 达到新平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是 ( )
N2O4(g),此时平衡混合气体中NO2的体积分数为x%;若再充入1mol N2O4,在温度不变的情况下, 达到新平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是 ( )
A.x>y B.x=y C.x<y D.不能确定
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源:2016-2017学年广西桂林十八中高二上期中文化学卷(解析版) 题型:填空题
下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
| IA |
| 0 | ||||||
1 | ① | II A |
| III A | IV A | V A | VI A | VIIA |
|
2 |
|
|
| ② | ③ |
|
|
| |
3 | ④ |
| ⑤ |
|
|
| ⑥ |
| |
请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为 ;
(2)②、③两元素的原子半径较大的是______________(填元素符号);
(3)④和⑤两种元素的金属性较强的是 (填元素符号);
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西桂林十八中高二上期中理化学卷(解析版) 题型:选择题
下列颜色变化与氧化还原反应无关的是
A.将乙醇滴入酸性K2Cr2O7溶液中,溶液由橙色变为绿色
B.将SO2通入滴有酚酞的NaOH溶液中,溶液红色褪去
C.将H2C2O4溶液滴入酸性KMnO4溶液中,溶液紫色褪去
D.将乙醛加入新制Cu(OH)2悬浊液中并加热至沸腾,出现红色沉淀
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:填空题
煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生 的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H1=+218.4kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4kJ/mol(反应I)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H2=-175.6kJ•mol-l(反应II)
CaS(s)+4CO2(g) △H2=-175.6kJ•mol-l(反应II)
请冋答下列问题:
(1)反应I能够自发进行的条件是____________。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应II的Kp=___________ (用表达式表示)。
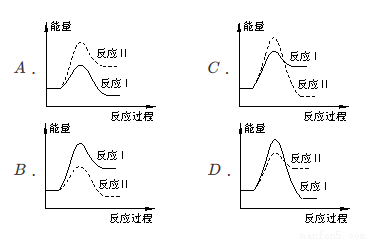
(3)假设某温度下,反应I的速率(v1)大于反应II的速率(v2),则下列反应过程能量变化示意图正确的是______________。
(4)通过监测反应体系中气体浓度的变化判断反应I和II是否同时发生,理由是___________。
(5)图I为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有__________。
A.向该反应体系中投入石灰石 B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数 D.提高反应体系的温度
(6)恒温恒容条件下,假设反应I和II同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)
随时间t变化的总趋势图。

查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:选择题
人体吸入CO后在肺中发生反应CO+HbO2 O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )
O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )
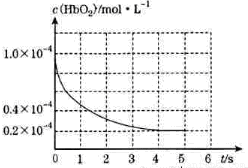
A.反应开始至4s内用HbO2表示的平均反应速率为2×l0-4mol/(L·s)
B.反应达平衡之前,O2与HbCO的反应速率逐渐减小
C.将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理
D.该温度下反应CO+HbO2 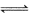 O2+HbCO的平衡常数为107
O2+HbCO的平衡常数为107
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:选择题
—定条件下,对于可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3 (均不为零),平衡时 X、Y、Z 的浓度分别为 0.1 mol / L、0.3 mol /L、0.08mol/L, 则下列判断正确的( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3 (均不为零),平衡时 X、Y、Z 的浓度分别为 0.1 mol / L、0.3 mol /L、0.08mol/L, 则下列判断正确的( )
A.c1:c2=3:1
B.平衡时.Y和Z的生成速率之比为2:3
C.X、Y的转化率不相等
D.c1的取值范围为0mol/L<c1<0.14mol/L
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:选择题
对于任何一个化学平衡体系,采取以下措施,一定会使平衡发生移动的是( )
A.加入一种反应物 B.增大体系压强 C.使用催化剂 D.升高温度
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
化学知识广泛应用于生产、生活中,下列叙述不正确的是
A.研发可降解高分子材料,减少“白色污染”
B.明矾和ClO2都能作为净水剂,其原理完全相同
C.海水淡化和工业生产及生活废水的再生利用,是解决缺水问题的有效途径
D.液氯罐泄漏时,可将其移入水塘中,并向水塘中加入生石灰
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:填空题
原子序数依次递增 且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子。回答下列问题:
且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子。回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为 ,Y2X2分子中σ键和π键个数比为 。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是 。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是 。
(4)元素W能形成多种配合物,如:W(CO)5等。
①基态W3+的M层电子排布式为 。
② W(CO)5常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断W(CO)5晶体属于 晶体(填晶体类型),该晶体中W的化合价为 。
W(CO)5常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断W(CO)5晶体属于 晶体(填晶体类型),该晶体中W的化合价为 。
(5)下列有关的说法正确的是 。
A.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
B.电负性顺序:X<Y<Z<Q
C.因为晶格能CaO比KCl高,所以KC l比CaO熔点低
l比CaO熔点低
D.H2 YO3的分子结构中含有一个非羟基氧,故其为中强酸
(6)Q和Na形成的一种只含有离子键的离子化合物的晶胞结构如图4,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a= pm。(用含ρ、NA的计算式表示)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com