

| �������� | Fe��OH��3 | Al��OH��3 | Mg��OH��2 |
| ��ʼ����pH | 1.5 | 3.3 | 9.4 |
���� ��1������ʯ���Կ�����MgO��FeO��Fe2O3��Al2O3��SiO2��ɣ�����ʯ�������ܽ��MgO��FeO��Fe2O3��Al2O3��HCl��Ӧ�ܽ⣬��SiO2��HCl����Ӧ�������ܽ⣻
��2������м���H2O2����Fe2+������Fe3+��Fe��OH��2������Fe��OH��3����ʱ��Һ�е�Fe3+��Al3+�����ʣ�����ȥFe3+��Al3+�Ĺ�����һ�����ܽ�Mg2+��ʧ��Ϊ�˴ﵽ���Ŀ�ģ�����������ʾӦ�õ�ԭ����Fe3++3H2O?Fe��OH��3+3H+��Al3++3H2O?Al��OH��3+3H+��ֻҪ����һ��������H+�����ʼ���ʹ����ˮ��ƽ��������Ӧ�����ƶ�����ȥFe3+��Al3+���÷���ʹ�ü�Ca��OH��2�ķ��������˲�����Ca��OH��2����̫�࣬�轫��Һ��pH������7��8����pHС��7��Al3+������ȫ��������pH���ߵ������ɵ�Al��OH��3�ַ�����ӦAl��OH��3+OH-=AlO2-+2H2O���ܽ⣬ͬʱMg2+Ҳת��Ϊ��������ʧ��
��3���ƴ���Fe2O3��Ӧ�Ƚ����к��е�����Al��OH��3��ȥ����ȥAl��OH��3�ķ�����������������ǿ������ʣ�
��4��ȷ����ƷaMgCO3•bMg��OH��2•cH2O��a��b��c��ֵ�������趨��������Ʒ���������Ԫ���غ����õ���
��� �⣺��1������ʯ�������ܽ⣬MgO��FeO��Fe2O3��Al2O3��HCl��Ӧ�ܽ⣬��Ӧ����ʽ�ֱ�Ϊ��MgO+2HCl=MgCl2+H2O��FeO+2HCl=FeCl2+H2O��Fe2O3+6HCl=2FeCl3+3H2O��Al2O3+6HCl=2AlCl3+3H2O����SiO2�������ᷴӦ���Գ�������ʽ��ȥ������Һ�����Mg2+��Al3+�⣬�����еĽ���������Fe3+��Fe2+��
�ʴ�Ϊ��Fe3+��Fe2+��
��2����ʱ��Һ�е�Fe3+��Fe2+��Al3+�����ʣ�����ȥFe3+��Fe2+��Al3+�Ĺ�����һ�����ܽ�Mg2+��ʧ��Ϊ�˴ﵽ���Ŀ�ģ��ȼ�������������Fe2+������Fe3+��Fe��OH��2������Fe��OH��3��H2O2�������ԣ�Fe3+�������ԣ�����м���H2O2������2Fe2++H2O2+2H+=2Fe3++2H2O������������ʾӦ�õ�ԭ����Fe3++3H2O?Fe��OH��3+3H+��Al3++3H2O?Al��OH��3+3H+��ֻҪ����һ��������H+�����ʼ���ʹ����ˮ��ƽ��������Ӧ�����ƶ�����ȥFe3+��Al3+���÷���ʹ�ü�Ca��OH��2�ķ��������˲�����Ca��OH��2����̫�࣬�轫��Һ��pH������7��8����pHС��7��Al3+������ȫ��������pH���ߵ������ɵ�Al��OH��3�ַ�����ӦAl��OH��3+OH-=AlO2-+2H2O���ܽ⣬ͬʱMg2+Ҳת��Ϊ��������ʧ��
�ʴ�Ϊ����Fe2+������Fe3+��Fe��OH��2������Fe��OH��3��2Fe2++H2O2+2H+=2Fe3++2H2O��Al��OH��3�ܽ⡢Mg2+������
��3���ƴ���Fe2O3��Ӧ�Ƚ����к��е�����Al��OH��3��ȥ����ȥAl��OH��3�ķ�����������������ǿ������ʣ�
Al��OH��3������ǿ��ʿ�A�м����������ƣ������������������Ʒ�Ӧ����ƫ�����ƣ�ƫ�������������̼��Ӧ������������������̼�����ƣ����˵õ�������������������������������������õ������������ӷ���ʽΪ��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��2Fe��OH��3$\frac{\underline{\;\;��\;\;}}{\;}$Fe2O3+3H2O
�ʴ�Ϊ��NaOH����������գ�
��4��m����Ʒ��=18.2g��m��CO2��=6.6g��m��MgO��=8.0g����ʽ̼��þ�ֽ⣺aMgCO3?bMg��OH��2?cH2O $\frac{\underline{\;����\;}}{\;}$��a+b��MgO+aCO2��+��b+c��H2O����
���������غ�ã�m��H2O��=18.2g-6.6g-8.0g=3.6g��
��m��MgO���T0.2mol��
n��CO2���T0.15mol��
n��H2O���T0.2mol��
�ã�a��b��c=0.15��0.05��0.15=3��1��3��
�ʴ�Ϊ��3��1��3��
���� ������Ҫ����Ԫ�ػ������н��������������ʣ�����ʱ��������֪���ʼ�ķ�Ӧԭ�����������������ʵ�����ƣ���Ŀ�ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a��0 | |
| B�� | �����¶ȣ������ʵ�Ũ�Ȳ��� | |
| C�� | �����¶ȣ�CO��ƽ��ת���ʽ��� | |
| D�� | ʹ�ô����ܼӿ췴Ӧ���ʲ���߷�Ӧ���ƽ��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{\;}^{12}$C��${\;}_{\;}^{14}$C��Ϊͬλ�� | |
| B�� | �Ҵ�������ѣ�CH3-O-CH3����Ϊͬ���칹�� | |
| C�� | ���������Ϊͬ�������� | |
| D�� | H2O��D2O��Ϊͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
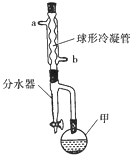 ��������������Ϊ�����㽶���桢ƻ���ȶ��ֿ�ζʳƷ�����ϣ�ʵ���Һϳ�������������ԭ������������촼[��CH3��2CHCH2CH2OH]����װ����ͼ��ʾ��
��������������Ϊ�����㽶���桢ƻ���ȶ��ֿ�ζʳƷ�����ϣ�ʵ���Һϳ�������������ԭ������������촼[��CH3��2CHCH2CH2OH]����װ����ͼ��ʾ��| ���� | ������ | ���� | ���촼 | |
| �е�/�� | 290 | 80.7 | 117.9 | 132.5 |
| �ܶ�/g•cm-3 | 1.26 | 0.78 | 1.05 | 0.81 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2O3�������� ���������� | B�� | H2SO3���� �� | ||
| C�� | CO2������̼ ���������� | D�� | Na2CO3���� �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1����3��Ϊ�û���Ӧ | |
| B�� | ��1����2����3����Ϊ������ԭ��Ӧ | |
| C�� | ��2��Ϊ���Ϸ�Ӧ | |
| D�� | ������Ӧ�ķ�Ӧ���й�Ԫ�ؾ�����ԭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | M����H+ | |
| B�� | FeO42-���������� | |
| C�� | ClO-�ڷ�Ӧ�б����� | |
| D�� | ����1mol FeO42-ʱ��ת��1.5mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com