
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1: 
(1)海藻灼烧时是将带其放入(填仪器名称)中,用酒精灯充分加热灰化.
(2)指出提取碘的过程中有关的实验操作名称:①②、 .
(3)用CCl4从碘水中提取碘经过操作②后,有机溶剂在(填“上”或“下”)层,有机层呈色.
(4)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出图2实验装置中的错误之处并改正: 
①
② .
【答案】
(1)坩埚
(2)过滤;萃取;分液
(3)下;紫红
(4)冷凝管进出水方向错误,应为下进上出;温度计位置错误,温度计的液泡在支管口处
【解析】解:(1)海藻灼烧时是将带其放入坩埚,用酒精灯充分加热灰化.所以答案是:坩埚.(2)分离难溶性固体和溶液采用过滤的方法,海藻灰难溶于水,碘离子易属于水,所以该操作为过滤,碘在有机溶剂中的溶解度大于在水溶液中的溶解度,所以可以采用萃取的方法萃取出碘水中的碘,然后采用分液的方法分离,所以答案是:过滤;萃取、分液;(3)碘易溶于四氯化碳和苯,且四氯化碳和苯都符合萃取剂选取标准,所以可以用四氯化碳或苯作萃取剂,如果选四氯化碳作萃取剂,四氯化碳密度大于水,所以有机层在下方,且溶液呈紫红色,如果选苯作萃取剂,苯密度小于水,在水的上方,且溶液呈紫红色,所以答案是:下、紫红;(4)冷凝水应是下进上出,冷凝水的方向错误,应为下进上出;温度计水银球的位置错误,温度计水银球应与烧瓶支管口相平;①冷凝管进出水方向错误,应为下进上出,所以答案是:冷凝管进出水方向错误,应为下进上出;②温度计位置错误,温度计的液泡在支管口处,所以答案是:温度计位置错误,温度计的液泡在支管口处;


科目:高中化学 来源: 题型:
【题目】下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物.试推断: 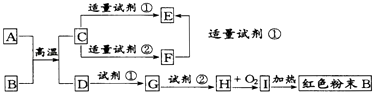
(1)写出物质的化学式:A:B:C:Ⅰ: .
(2)向F中逐滴滴加试剂①的现象为 .
(3)写出下列反应的方程式: C→E的离子方程式
C→F的离子方程式
G→H的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲和乙的某些性质如表所示:
物质 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 水中的溶解性 |
甲 | -98 | 37.5 | 0.93 | 可溶 |
乙 | -48 | 95 | 0.90 | 可溶 |
现有甲和乙的混合物,进行分离时,可采用的方法是( )
A.过滤B.蒸发C.蒸馏D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸(化学式用H2B表示)在水中的电离方程式是H2B===H++HB-;HB-![]() H++B2-。回答下列问题。
H++B2-。回答下列问题。
(1)Na2B溶液显_____(填“酸性”、“中性”或“碱性”),理由是_______(用离子方程式表示)。
(2)在0.1 mol·L-1的Na2B溶液中,下列粒子浓度关系式正确的是____。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
D.c(Na+)=2c(B2-)+2c(HB-)
(3)已知0.1 mol·L-1 NaHB溶液的pH=2,则0.1 mol·L-1 H2B溶液中的氢离子的物质的量浓度可能____0.11 mol·L-1(填“<”、“>”或“=”),理由是_____。
(4)0.1 mol·L-1 NaHB溶液中各种离子浓度由大到小的顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,1体积水溶解700体积氨气,所得溶液密度为0.9gcm﹣3 , 这种氨水的物质的量浓度和溶质的质量分数分别为( )
A.18.4molL﹣134.7%
B.20.4molL﹣138.5%q2
C.18.4molL﹣138.5%
D.20.4molL﹣134.7%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e﹣、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系: 
①均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;
②均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应.请回答下列问题:
(1)化合物甲的电子式为 .
(2)F元素在周期表中的位置稳定性:A2CA2E(填“大于”“小于”“等于”).
(3)均含有D元素的乙与丁在溶液中发生反应的离子方程式
(4)丙、丁分别是含F元素的简单阳离子,检验含丙、丁两种离子的混合溶液中的低价离子,可以用酸性KMnO4溶液,其对应的离子方程式为:
(5)已知常温下化合物FE的Ksp=6×10﹣18 mol2L﹣2 , 常温下将1.0×10﹣5molL﹣1的Na2E溶液与含FSO4溶液按体积比3:2混合,若有沉淀F E生成,则所需的FSO4的浓度要求 . (忽略混合后溶液的体积变化).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s) =Ag(s)+Cl(AgCl) [Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着 Cl(AgCl)+e-→Cl-(aq),若将光源移除,电池会立即恢复至初始状态。下列说法正确的是
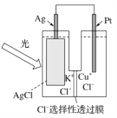
A. 光照时,电流由 铂流向银
B. 光照时,Pt 电极发生的反应为 2Cl-+2e-= Cl2
C. 光照时,Cl-向 Ag 电极移动
D. 光照时,电池总反应:AgCl (s)+Cu+(aq)=Ag(s)+Cu2+(aq)+Cl-(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com