
| A. | 镁、NaOH溶液 | B. | 铜、稀硫酸 | C. | 锌、浓硝酸 | D. | 铁、FeCl3 |
分析 某含有铝电极的原电池工作时,电子从铝电极上流出吗,则金属铝是负极,正极材料的活泼性比金属铝弱,电解质和金属铝之间可以发生自发氧化还原反应即可.
解答 解:含有铝电极的原电池工作时,电子从铝电极上流出吗,则金属铝是负极,正极材料的活泼性比金属铝弱,电解质和金属铝之间可以发生自发氧化还原反应.
A、镁、Al、NaOH溶液能够成原电池,金属铝是负极,故A不选;
B、铜、铝、稀硫酸溶液能够成原电池,金属铝是负极,故B不选;
C、锌、Al、浓硝酸溶液能够成原电池,金属铝是正极,故C选;
D、铁、FeCl3、Al能够成原电池,金属铝是负极,故D不选;
故选C.
点评 本题考查学生原电池的构成条件以及负极的判断,不是活泼金属一定做负极,电子流出的极是负极,难度中等.


科目:高中化学 来源: 题型:解答题
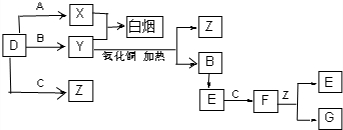
 ,E的化学式为NO.
,E的化学式为NO.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
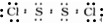 .
.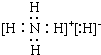 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

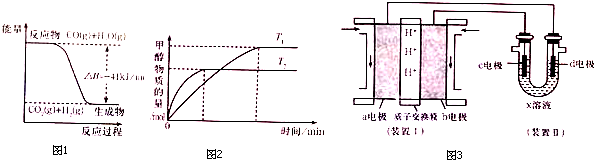
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “加碘食盐”、“含氟牙膏”、“富硒营养品”、“高钙牛奶”、“加铁酱油”等等,这里的碘、氟、硒指的是对应的单质分子,而钙、铁则指的是对应的钙离子和铁离子 | |
| B. | 淀粉及做衣服的棉和麻均为天然高分子化合物 | |
| C. | 煎炸食物的花生油和牛油都是可水解的饱和酯类 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
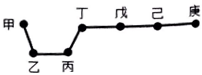 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )| A. | 甲一定是金属元素 | |
| B. | 气态氢化物的稳定性:庚>己>戊 | |
| C. | 乙、丙、丁的最高价氧化物水化物可以以相互反应 | |
| D. | 庚的最高价氧化物水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 4种 | C. | 3种 | D. | 2种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com