
下列叙述正确的是
A.光导纤维中所用材料为晶体硅
B.SiO2是酸性氧化物, 所以不与任何酸反应
C.可用Na2SiO3溶液和CO2反应来制备H2SiO3
D.NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中
科目:高中化学 来源:2014-2015江苏省扬州市高一上学期期末化学试卷(解析版) 题型:实验题
(12分)利用硫酸厂烧渣(含铁的氧化物和少量FeS及SiO2)制碱式硫酸铁的流程如下:
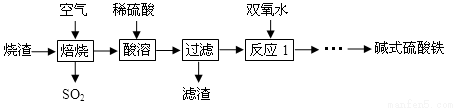
(1)SO2与过量NaOH溶液反应的离子方程式为 。
(2)滤渣的主要成分为 (填化学式)。
(3)反应1中加双氧水的目的是 。
(4)碱式硫酸铁的化学式为Fex(OH)y(SO4)z·nH2O,为确定其组成进行如下实验:
①称取1.6920 g 样品溶于足量的稀盐酸中;
②加足量的BaCl2溶液,过滤、洗涤、干燥、称重,得固体质量为2.3300 g;
③向步骤②的滤液中加过量的NaOH溶液,过滤、洗涤、灼烧、称重,得固体质量为0.6400 g。
根据以上实验数据计算碱式硫酸铁样品中的n(OH-): n(SO42-)(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省扬州市高二上学期期末化学(必修)试卷(解析版) 题型:选择题
以下食品中的有机成分属于高分子化合物的是
A.谷类中含有的淀粉 B.植物油、动物脂肪中含有的油脂
C.食醋中含有的醋酸 D.酒中含有的酒精
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:填空题
(9分)试用化学方法除去下列物质中混有的少量杂质,要求除杂试剂均过量,若为溶液中的离子反应请写出其离子方程式,否则写化学方程式。并写出相应的分离方法。
(1)除去FeCl2溶液中混有的少量FeCl3;方程式: ______________ 。分离方法:______
(2)除去CO2气体中混有的少量HCl;方程式: _______________。分离方法:______
(3)除去NaCl溶液中混有的少量NaBr;方程式:__________________ 。分离方法:______
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:选择题
将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,明显不正确的是
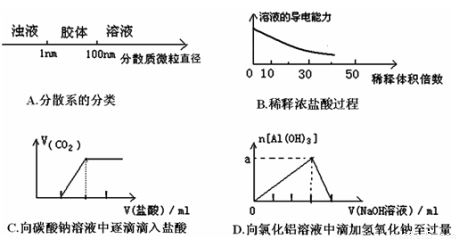
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:选择题
下列说法中正确的是
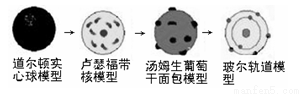
A.40K与40Ca原子中的中子数相等
B.互为同位素的两种核素,它们原子核内的质子数一定相等
C.人们发现了112种元素,即共有112种核素
D.原子结构模型演变历史可以表示为上图
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省新余市高一上学期期末考试化学试卷(解析版) 题型:实验题
如图中,A是氯气的发生装置,B、C是净化气体的装置,B装置中装有饱和食盐水,D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置。
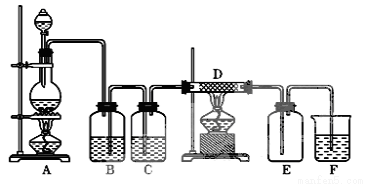
(1)上述装置中有一处错误,请指出是 处(用字母表示)。
(2)B装置的作用是 ,C装置中需要加入 。
(3)写出A中发生反应的离子方程式 ,写出D中发生反应的化学方程式 。
(4)如果A中产生氯气3.36L(标准状况),请计算:被氧化的HCl的物质的量 。
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省新余市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.向Al2(SO4)3溶液中加入过量的氨水:Al3++4NH3·H2O =AlO2—+ 4NH4++2H2O
B.铁与稀盐酸反应: 2Fe+6H+ = 2Fe3++3H2↑
C.氢氧化钡和稀硫酸: Ba2++2OH—+2H++SO42—=BaSO4↓+2H2O
D.将钠加入水中: Na+2H2O=Na++2OH—+H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:实验题
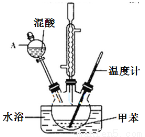
某实验小组用下图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯)
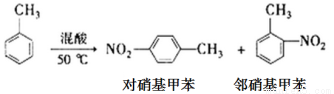
反应原理:
实验步骤:①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40mL;
②在三颈瓶中加入13g甲苯(易挥发),按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸;
④控制温度约为50℃-55℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到对硝基甲苯和邻硝基甲苯共15g。
相关物质的性质如下:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
(1)仪器A的名称是________。
(2)配制混酸的方法是 。
(3)若实验后在三颈瓶中收集的产物较少,可能的原因是: 。
(4)本实验采用水浴加热,水浴加热的优点是 。
(5)分离反应后产物的方案如下:

操作1的名称是 ,操作2中不需要用到下列仪器中的 。(填序号)
a.冷凝管
b.酒精灯
c.温度计
d.分液漏斗
e.蒸发皿
(6)本实验中邻、对硝基甲苯的产率为________(结果保留小数点后一位数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com