
【题目】乙炔是重要的有机化工原料,其化学性质活泼。完成下列填空
(1)乙炔能使溴水褪色,说明乙炔能发生__________ 反应(填反应类型);乙炔能使酸性高锰酸钾褪色,说明乙炔容易被_____________。
(2)乙炔在一定条件下三聚得到CH2=CH—C≡C—CH=CH2,写出与该三聚物具有相同化学式且不易发生加成反应的物质的结构简式 :___________________________。
(3)写出苯与液溴反应的方程式:________________________________________。
(4)鉴别苯和二乙烯基乙炔(CH2=CH—C≡C—CH=CH2)可用的试剂_________________________。
(5)乙炔聚合得到聚乙炔,聚乙炔_________导电(选填“能”或“不能”)。
(6)乙炔在不同的催化条件下加氢可得到不同的产物。下列物质与乙炔加氢得到的某种产物互为同系物的是________________(选填编号)。
a.C2H4 b.C2H6 c.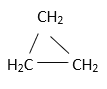 d.CH2=CHCH3
d.CH2=CHCH3
【答案】加成 氧化 
![]() 酸性高锰酸钾溶液或溴水 能 d
酸性高锰酸钾溶液或溴水 能 d
【解析】
(1)乙炔能使溴水褪色,是因为乙炔中含有碳碳双键,能够与溴水发生加成反应;乙炔能使酸性高锰酸钾褪色,是因为乙炔中含有碳碳双键,被高锰酸钾氧化;
故答案为:加成;氧化;
(2)CH2=CH-C≡C-CH=CH2的分子式为C6H6,不饱和度为4,不易发生加成反应,说明不含有典型的双键、三键,所以结构简式为 ;
;
故答案为: ;
;
(3)苯与液溴反应生成溴苯和溴化氢,反应的化学方程式为:![]() ;
;
(4)苯不能使酸性高锰酸钾溶液或溴水褪色,二乙烯基乙炔(CH2=CH—C≡C—CH=CH2)能使酸性高锰酸钾溶液或溴水褪色,鉴别苯和二乙烯基乙炔(CH2=CH—C≡C—CH=CH2)可用的试剂酸性高锰酸钾溶液或溴水;
(5)乙炔生成聚乙炔:nC2H2![]()
![]() ,聚乙炔中碳碳单键、碳碳双键交替出现,具有电子容易流动的性质,所以能导电;
,聚乙炔中碳碳单键、碳碳双键交替出现,具有电子容易流动的性质,所以能导电;
故答案为:能;
(6)乙炔在不同的催化条件下加氢可得到乙烯、乙烷,而C2H4为乙烯,C2H6为乙烷,![]() 与乙烯、乙烷的结构都不相似,不属于同系物,CH2=CHCH3与乙烯结构相似,在分子组成上相差1个CH2,属于同系物,故选:d。
与乙烯、乙烷的结构都不相似,不属于同系物,CH2=CHCH3与乙烯结构相似,在分子组成上相差1个CH2,属于同系物,故选:d。


科目:高中化学 来源: 题型:
【题目】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O),流程如下:
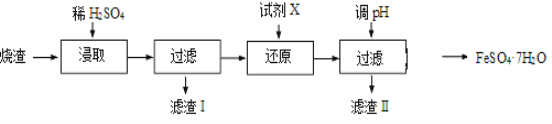
(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为__________________。能提高烧渣浸取速率的措施有__________________(填字母)。
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
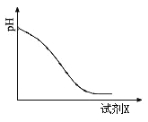
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是________(填字母)。还原结束时,溶液中的主要阴离子有_____________。
A.Fe粉 B.SO2 C.NaI
(3)滤渣Ⅱ主要成分的化学式为__________________;由分离出滤渣Ⅱ后的溶液得到产品,进行的操作是_______________________________ 、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:

请回答下列问题:
(1)向操作①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有______(填离子符号)。
(2)操作②中反应的离子方程式:__________________________________。
(3)操作③中反应的离子方程式:__________________________________。
(4)操作④中一系列处理的操作步骤:过滤、______、灼烧、_______、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为______g。(用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(省略夹持装置,气密性已检查)如图所示。下列推断不合理的是( )
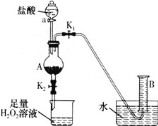
A.烧杯中H2O2溶液的作用是将Fe2+氧化为Fe3+
B.A中存在氧化铁与盐酸反应生成氯化铁的反应
C.利用B装置不能准确测量生成氢气的体积
D.将反应后的溶液放入烧杯中再通入少量SO2,则溶液颜色立即由棕黄色变为浅绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的反应装置如图所示。下列实验操作或叙述错误的是( )。
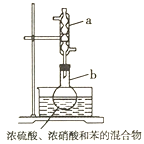
A.实验时水浴温度需控制在50~60℃
B.加入试剂的顺序:先加浓硝酸,再加浓硫酸,最后加入苯
C.仪器![]() 的作用:冷凝回流苯和硝酸,提高原料的利用率
的作用:冷凝回流苯和硝酸,提高原料的利用率
D.完全反应后,可用仪器![]() 、
、![]() 蒸馏得到产品
蒸馏得到产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以电石(主要成分是CaC2)为原理制备乙炔,装置如图所示。完成下列填空:
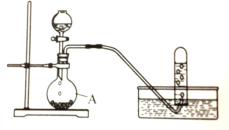
(1)仪器A的名称是______________。
(2)实验室制取乙炔的化学方程式为:___________________________________ 。
(3)为避免电石和水反应过于激烈,除用饱和食盐水代替水外,还需采取的措施是:__________。
(4)为除去乙炔中混有的少量硫化氢杂质,可将气体通过____________(选填编号)。
a.酸性KMnO4溶液 b.CCl4 c.NaOH溶液
(5)乙炔属于_______________(填“饱和烃”或“不饱和烃)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究小组的同学们以甲苯和乙醇为主要原料,按下列路线合成一种重要的医药中间体——乙酰基扁桃酰氯。

已知: ;
;![]() ;
;![]()
(1)甲苯与氯气反应生成![]() 的条件是______;
的条件是______;![]() 中含有的官能团是_____;
中含有的官能团是_____;![]() 的结构简式是____。
的结构简式是____。
(2)下列说法正确的是______。
a 化合物![]() 不能发生取代反应
不能发生取代反应
b 乙酰基扁桃酰氯属于芳香烃
c 化合物![]() 能与新制的
能与新制的![]() 发生反应
发生反应
(3)![]() 的化学方程式是________。
的化学方程式是________。
(4)化合物![]() 有多种同分异构体,同时符合下列条件的同分异构体共有__种,写出其中一种同分异构体的结构简式____。
有多种同分异构体,同时符合下列条件的同分异构体共有__种,写出其中一种同分异构体的结构简式____。
①红外光谱检测表明分子中含有氰基(![]() );②核磁共振氢谱检测表明分子中有苯环,且苯环上有两种不同化学环境的氢原子。
);②核磁共振氢谱检测表明分子中有苯环,且苯环上有两种不同化学环境的氢原子。
(5)参照上述流程图,以乙醇为原料制备![]() ,设计合成路线____:(无机试剂任选)。
,设计合成路线____:(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到目的的是( )

A. 装置①依据两容器内气体颜色变化,不能判断反应2NO2(g)![]() N2O4(g)平衡移动的方向
N2O4(g)平衡移动的方向
B. 装置②依据U管两边液面的高低判断Na和水反应的热效应
C. 装置③测定中和热
D. 装置④依据褪色快慢比较浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸和硫酸镁是重要的化工原料。以硼铁混精矿[主要成分为MgBO2(OH)、UO2和Fe3O4,还有少量的Fe2O3、FeO、SiO2]为原料制备硼酸和硫酸镁的工艺流程如下:
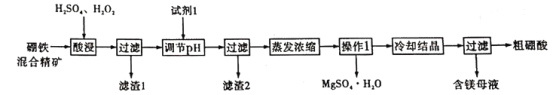
已知:①UO22+在pH为4-5的溶液中生成UO2(OH)2沉淀;②Fe2+和Fe3+沉淀完全的pH分别为9.7、3.7。
(1)酸浸过程中MgBO2(OH)与硫酸反应的离子方程式为_____。
(2)酸浸过程中加入H2O2的目的是______(写出两条),滤渣1的主要成分是___(填化学式)。
(3)试剂1最好选择_____(填化学式)。若调节溶液pH前,溶液中c(Mg2+)=0.2 mol/L,当溶液pH调至5时,UO2+沉淀完全,此时是否有Mg(OH)2沉淀生成____。{通过计算说明,Ksp[Mg(OH)2]=5.6×10-12}
(4)操作1的名称是_____。
(5)MgSO4·H2O加热脱水可以得无水MgSO4,那么MgCl2·6H2O晶体直接加热___(填“能”或“不能”)得到无水MgCl2,理由是_______。
(6)已知:H2CO3的Ka1=4.4×10-7,Ka2=4.7×10-11;H3BO3的Ka=5.8×10-10。向碳酸钠溶液里逐滴加入硼酸溶液____(填“有”或“无”)气泡产生,理由是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com