
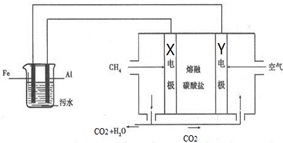
 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.模拟处理装置如图所示,下列说法错误的是( )
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.模拟处理装置如图所示,下列说法错误的是( )| A、X电极是负极,电极反应式为:CH4-8e-+4CO32-═5CO2+2H2O |
| B、铁是阳极,失去电子生成Fe2+ |
| C、工作时熔融盐中的碳酸根移向Y电极 |
| D、污水中存在反应:4Fe2++10H2O+O2═4Fe(OH)3↓+8H+ |


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
| A、溴、碘单质和CCl4中都含有卤素 |
| B、溴、碘是单质,CCl4是化合物 |
| C、Cl2、Br2、I2是非极性分子,CCl4也是非极性分子,而水为极性分子 |
| D、以上说法都不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水分子间的作用力强于分子内的H-O键 |
| B、形成化学键的微粒只能是离子 |
| C、含有离子键的化合物一定是离子化合物 |
| D、共价化合物分子里的化学键只能是极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知HF的共价键键能比HCl大,说明稳定性:HF>HCl | ||||
| B、已知正反应的活化能大于逆反应的活化能,说明总能量:生成物>反应物 | ||||
| C、已知NaClO+SO2+H2O→HClO+Na2SO3,说明给出质子能力:HSO3->HClO | ||||
D、已知CaCO3+SiO2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、T℃时,两饱和溶液中c(Ca2+):CaCO3>CaF2 |
| B、T℃时,两饱和溶液等体积混合,会析出CaF2固体 |
| C、T℃时,CaF2固体在稀盐酸中的Ksp比在纯水中的Ksp大 |
| D、T℃时,向CaCO3悬浊液中加NaF固体,可能析出CaF2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大;x2-和Y+有相同的核外电子排布;Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气态单质.回答下列问题(相关回答均用元素符号或化学式表示):
X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大;x2-和Y+有相同的核外电子排布;Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气态单质.回答下列问题(相关回答均用元素符号或化学式表示):查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-H | C=C | C-C | H-H |
| 键能/kJ?mol-1 | 414.4 | 615.3 | 347.4 | 435.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 和
和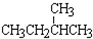 ; ②
; ②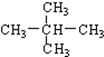 和
和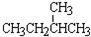 ;
;| 类别 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com