
(12分)请根据下图作答:

已知:一个碳原子上连有两个羟基时,易发生下列转化:
(1)E中含有的官能团是
(2)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B的分子式为 。
(3)反应③的化学方程式 。
(4)F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G可能有_______种结构,写出其中不含甲基的同分异构体的结构简式__________________________。
(1)羧基; (2)C10H10O2(3)CH3CHO+2Cu(OH)2 CH3COOH+Cu2O+2H2O;
CH3COOH+Cu2O+2H2O;
(4)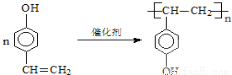 (5)四;
(5)四;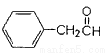
【解析】
试题分析:根据题给流程和信息知,A[CH3COOCH(Cl)CH3]在碱性条件下发生水解生成C和D,C能与新制氢氧化铜在加热条件下反应,则C为CH3CHO,D为CH3COONa,E为CH3COOH,B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B分子中a=b,12a+a+2×16=162,a=10,则B的分子式为C10H10O2,水解生成F和CH3COOH,则F中应有8个C原子,又知:①能跟FeCl3溶液发生显色反应,说明分子中含有酚羟基;②能发生加聚反应,说明分子中含有碳碳双键;③苯环上的一氯代物只有两种,说明两个取代基应在对位位置,F应为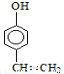 ,则B为
,则B为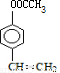 。(1)E为CH3COOH,含有的官能团是羧基;(2)B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B分子中a=b,12a+a+2×16=162,a=10,则B的分子式为C10H10O2;(3)反应③为乙醛和新制氢氧化铜发生氧化反应生成乙酸、氧化亚铜和水,化学方程式为
。(1)E为CH3COOH,含有的官能团是羧基;(2)B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B分子中a=b,12a+a+2×16=162,a=10,则B的分子式为C10H10O2;(3)反应③为乙醛和新制氢氧化铜发生氧化反应生成乙酸、氧化亚铜和水,化学方程式为
CH3CHO+2Cu(OH)2 CH3COOH+Cu2O+2H2O;(4)F为
CH3COOH+Cu2O+2H2O;(4)F为 ,在一定条件下发生加聚反应的化学方程式为
,在一定条件下发生加聚反应的化学方程式为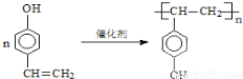 ;(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应,说明分子中含有-CHO,可为甲基苯甲醛(有邻、间、对3种)和苯乙醛,共四种,不含甲基的同分异构体的结构简式为
;(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应,说明分子中含有-CHO,可为甲基苯甲醛(有邻、间、对3种)和苯乙醛,共四种,不含甲基的同分异构体的结构简式为 。
。
考点:考查有机推断,涉及官能团的识别和性质,同分异构体、化学方程式的书写。


科目:高中化学 来源:2013-2014河北省保定市第二学期期中考试高二化学试卷(解析版) 题型:选择题
香豆素﹣4是一种激光染料,应用于可调谐染料激光器。香豆素﹣4由C、H、O三种元素组成,分子球棍模型如右图所示,下列有关叙述正确的是( )

① 分子式为C10H9O3 ② 能与Br2水发生取代反应
③ 能与Br2水发生加成反应 ④ 能使酸性KMnO4溶液褪色
⑤ 1mol香豆素﹣4最多能与含2molNaOH的溶液反应
A. ①②③ B. ③④⑤ C. ②③④ D. ② ③④⑤
③④⑤
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省保定市第二学期期中考试高一化学试卷(解析版) 题型:选择题
下列叙述表示可逆反应N2 + 3H2  2NH3一定处于平衡状态的是……… ( )
2NH3一定处于平衡状态的是……… ( )
A.N2、H2、NH3的百分含量相等 B.3v(N2)正= v(H2)逆
C.定容容器中,气体的密度不变 D.N2、H2、NH3的浓度之比为1:3:2
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省鹰潭市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
[化学——选修3:物质结构与性质](15分)
已知元素A、B、C、D、E、F均属前四周期且原子序数依次增大, 其中A含有3个能级,且每个能级所含的电子数相同,C的基态原子2p轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F除最外层原子轨道处于半充满状态,其余能层均充满电子,请回答下列问题:
(1)元素A、B、C的第一电离能由小到大的是_______(用元素符号表示)。
(2)F原子的外围电子排布式为_______,F的晶体中原子的堆积方式是下图中的_______(填写“甲”、“乙”或“丙”)。

(3)B与C形成的四原子阴离子的立体构型为 ,其中B原子的杂化类型是 。
(4)任写一种与AB-离子互为等电子体的离子 。
(5)F(OH)2难溶于水,易溶于氨水,写出其溶于氨水的离子方程式 。
(6)D和E形成的化合物的晶胞结构如图,其化学式为 ,
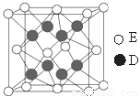
已知晶体的密度为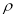 g·cm-3,阿伏加德罗常数为NA,
g·cm-3,阿伏加德罗常数为NA,
则晶胞边长a= cm。(用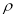 、NA的计算式表示)
、NA的计算式表示)
(7)A、B、C三种元素和氢元素形成的氰酸有两种结构,一种分子
内含有叁键,称为氰酸,另一种分子内不含叁键,称为异氰酸,
且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。请分别写
出氰酸和异氰酸的结构式:_______________、______________。
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省鹰潭市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②向100 mL0.1 mol/L 的溴化亚铁溶液中通入0.05 mol的氯气时发生反应的离子方程式:
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
③斜长石KAlSi3O8的氧化物形式可表示为:K2O?Al2O3?3SiO2
④酸性条件下KIO3溶液与KI溶液发生反应生成I2时的离子方程式:
IO3-+5I-+3H2O=I2+6OH-
⑤碳酸氢根离子的电离方程式可表示为:
⑥元素周期表中,从上到下,卤族元素的非金属性逐渐减弱,氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放
热19.3kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) △H= -38.6 kJ·mol-1
2NH3(g) △H= -38.6 kJ·mol-1
A.全部 B.②⑤ C.②③④⑦ D.②④⑦
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省鹰潭市下学期期末质量检测高二化学试卷(解析版) 题型:选择题
下列离子方程式与所述事实相符且正确的是( )
A.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
B.向Na2SO3溶液中通入足量氯气:SO32-+Cl2+H2O=SO42-+2Cl-+2H+
C.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O
D.钠与CuSO4溶液反应:2Na+Cu2+===Cu+2Na+
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省鹰潭市下学期期末质量检测高二化学试卷(解析版) 题型:选择题
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是 ( )
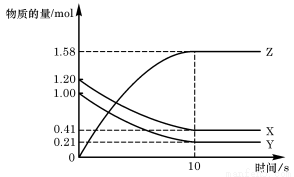
A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B.反应开始到10s, X的物质的量浓度减少了0.79mol/L
C.反应开始时10s, Y的转化率为79.0%
D.反应的化学方程式为:X(g)+ Y(g) Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省鹰潭市下学期期末质量检测高一化学试卷(解析版) 题型:选择题
反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
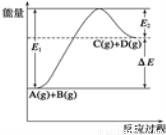
A.1molA与1molB充分反应后,能量变化为ΔE
B.加入催化剂后,反应加快,ΔE减小
C.反应物的总键能小于生成物的总键能
D.反应达到平衡时,升高温度,A的转化率增大
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省协作体高三第二次联考理综化学试卷(解析版) 题型:填空题
【化学—选修2:化学与技术】(15分)
化学是人类进步的关键,化学为人类的生产、生活提供了物质保证。
Ⅰ.氮的化合物是重要的化工产品。其生产方法也在逐渐改进中,各国科学家均在为提高其产量,降低能耗做各种有益的探究。
(1)25℃时合成氨反应热化学方程式为:N2(g)+3H2(g)==2NH3(g),ΔH=-92.4kJ/mol 。 在该温度时,取1molN2和3molH2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4kJ。其原因是_________________________________。
(2)近年有人将电磁场直接加在氮气与氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较好的产率。从化学反应本质角度分析,电磁场对合成氨反应的作用是 ;与传统的合成氨的方法比较,该方法的优点是 。
Ⅱ.(3)卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品。从卤水中提取镁的步骤为:
a.将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
b.将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
c.在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2·6H2O;
d.将MgCl2·6H2O在一定条件下加热得到无水MgCl2;
e.电解熔融的氯化镁可得到Mg。
①步骤d中的“一定条件”指的是 。
②有同学认为:步骤b后可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,你同意该同学的想法吗?为什么?
(4) 铀是核反应最重要的燃料,已经研制成功一种螫合型离子交换树脂,它专门吸附海水中 的U4+,而不吸附其他元素。其反应原理为 (树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com