
 ×1010(2分)
×1010(2分)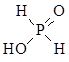 (或
(或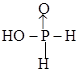 )(2分)
)(2分)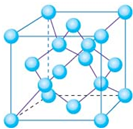 。所以金刚石的一个晶胞中含有的碳原子数=8×
。所以金刚石的一个晶胞中含有的碳原子数=8×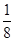 +6×
+6×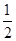 +4=8,因此立方氮化硼晶胞中应该含有4个N和4个B原子。设B-N键长为x,立方体的边长是a,则(4x)2=a2+2a2,解得x=
+4=8,因此立方氮化硼晶胞中应该含有4个N和4个B原子。设B-N键长为x,立方体的边长是a,则(4x)2=a2+2a2,解得x=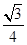 a。又因为
a。又因为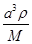 ×NA=4,解得a=
×NA=4,解得a=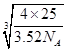 ,所以B-N键长是
,所以B-N键长是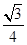
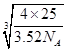 cm=
cm=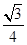
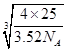 ×1010pm。
×1010pm。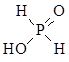 (或
(或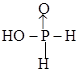 )。
)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



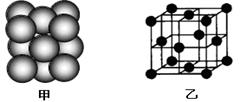
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
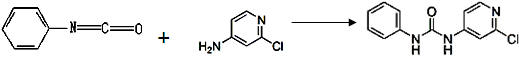
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O | 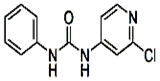 | 白色结晶粉末 | 170~172℃ | 易溶于水 |
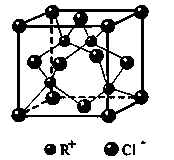
| | X | Y | Z |
| 第一电离能(kJ/mol) | 520.2 | 495.8 | 418.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


| A.离子键 | B.极性键 | C.非极性键 | D.配位键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
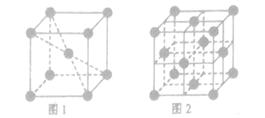
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,反应涉及到的物质中,X属于 晶体(填 晶体类型),MgO晶体的熔点比CaO高,主要原因是 。
,反应涉及到的物质中,X属于 晶体(填 晶体类型),MgO晶体的熔点比CaO高,主要原因是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 ,该氯化物的化学式为__________。
,该氯化物的化学式为__________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.O2和O3互为同位素 | B.O2转化为O3为化学变化 |
| C.相同物质的量的O2和O3的体积相同 | D.相同质量的O2和O3含有相同的分子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com