
【题目】向等物质的量浓度的ZnSO4和CuSO4的混合溶液中,逐滴加入1.5 mol·L1的Na2S溶液直至溶液中无沉淀产生,然后过滤。已知:Ksp(ZnS)=2.0×1022,Ksp(CuS)=1.3×1036。下列说法不正确的是
A.先生成CuS后生成ZnS沉淀,属于沉淀的转化
B.当ZnS沉淀完全时,溶液中![]() =6.5×1015
=6.5×1015
C.过滤得到的沉淀是CuS和ZnS的混合物
D.过滤后得到的溶液中仍有极少量的Cu2+和Zn2+
科目:高中化学 来源: 题型:
【题目】对于反应:4CO(g)+2NO2(g)= 4CO2(g)+N2(g) △H=-1200 kJ· mol-1,温度不同 (T2>T1)其他条件相同时,下列图像正确的是( )

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将pH=1的硫酸溶液平均分成两等份,一份加入适量水,另一份加入与该硫酸溶液物质的量浓度相同的氢氧化钠溶液(设混合后溶液体积等于混合前两液体体积之和),两者pH都升高了1,则加入水和加入NaOH溶液的体积比约为( )
A.11:1 B.10:1 C.6:1 D.5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20mL0.1000mol·L-1H2C2O4溶液中滴加0.1000mol·L-1NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化如图所示。下列有关叙述错误的是

A. 忽略H2C2O4的第二步电离,由题给信息,可以计算出常温下H2C2O4的电离常数
B. A、B、C三点所对应的溶液中,水的电离程度最小的是A点
C. A、B、C三点所对应的溶液中,均有c(Na+)<c(OH-)+c(HC2O4-)+2c(C2O42-)
D. 在B点溶液中,生成的含钠化合物有两种,且n(HC2O4-)+n(C2O42-)=2.0×10-3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施能明显增大原反应的化学反应速率的是( )
A.Na与水反应时增大水的用量
B.将稀H2SO4改为98%的浓H2SO4与Zn反应制取H2
C.在H2SO4与NaOH两溶液反应时,增大压强
D.恒温恒容条件下,在工业合成氨反应中,增加氮气的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
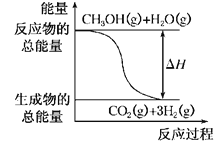
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
下列说法正确的是( )
A.CH3OH的燃烧热为-192.9 kJ·mol-1
B.反应①中的能量变化如上图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.由②推知反应CH3OH(l)+![]() O2(g)=CO2(g)+2H2(g)ΔH >-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH >-192.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液由水电离的c(OH-)=1×10-13mol/L,对于该溶液的叙述正确的是( )
A.溶液一定显酸性 B.溶液一定显碱性
C.溶液可能显中性 D.溶液可能是pH=13的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原滴定实验与中和滴定类似,是用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之。现用0. 00lmol/L酸性KMnO4溶液滴定未知浓度的NaHSO3溶液,请回答下列问题:
(1)完成滴定的离子方程式(在__中填系数,在___上填物质或离子):_____
____MnO4-+____HSO3-+____=____Mn2++___ ____+___H2O
(2)该滴定实验的仪器除了铁架台、滴定管夹外,还需要下列用品中的_____(填序号)
A.酸式滴定管 B.碱式滴定管 C.漏斗 D.锥形瓶 E.烧杯 F.白纸
(3) KMnO4溶液不能用____(酸、碱)式滴定管盛装,原因是:_______。
(4)是否需要选择指示剂?_____。滴定终点的现象是___________。
(5)滴定前平视KMnO4液面,刻度为amL,滴定后俯视液面刎度为bmL,则(b-a)mL比实际消耗KMnO4溶液体积_______(填“大”、“小”或“无影响”,下同)。根据(b-a) mL计算,得到NaHSO3的浓度比实际的浓度_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜在生产、生活中应用广泛。某化工厂用含少量铁的废铜渣为原料生产胆矾的流程如下:(已知:Fe3+在PH=3.7时就完全生成氢氧化铁沉淀)

(1)“浸出”时,原料中的铜均转化为硫酸铜。写出相应的化学方程式:________________。
(2)取样检验是为了确认Fe3+是否除尽,你的检验方法是________________
(3)调节pH的目的是____________。从滤液到胆矾应采用_________________过滤。
(4)气体a可以被循环利用,用化学方程式表示其被循环利用的原理为:2NO+O2=2NO2、_________________
(5)在农业上,将胆矾、生石灰和水按一定比例混合制成波尔多液,其反应的化学方程式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com