
判断下列说法是否正确,正确的划“√”,错误的划“×”
(1)氢键是氢元素与其他元素形成的化学键( )
(2)可燃冰(CH4·8H2O)中甲烷分子与水分子间形成了氢键( )
(3)乙醇分子和水分子间只存在范德华力( )
(4)碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键( )
(5)水分子间既存在范德华力,又存在氢键( )
(6)氢键具有方向性和饱和性( )
(7)H2和O2之间存在氢键( )
(8)H2O2分子间存在氢键( )
(9)卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大( )
(10)氢键的存在一定能使物质的熔、沸点升高( )
(11)极性分子中可能含有非极性键( )
(12)H2O比H2S稳定是因为水分子间存在氢键( )
答案 (1)× (2)× (3)× (4)× (5)√ (6)√ (7)× (8)√ (9)× (10)× (11)√ (12)×
解析 (1)氢键与氢有关但不属于化学键。
(2)可燃冰中水分子间存在氢键,但CH4与H2O之间不存在氢键。
(3)乙醇分子、水分子中都有—OH,符合形成氢键的条件。
(4)HI分子间只存在范德华力的作用。
(5)和(6)正确。
(7)H2与O2分子中的共价键均为非极性键,分子间只存在范德华力。
(8)H2O2分子中的H几乎成为“裸露”的质子,与水分子一样,H2O2分子间也存在氢键。
(9)卤素氢化物中,HF的熔、沸点最高。
(10)分子内氢键对物质的熔、沸点影响很小。
(11)在极性分子H2O2中存在非极性键。
(12)H2O比H2S稳定是O—H键键能大于S—H键键能,而与氢键无关。


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案科目:高中化学 来源: 题型:
下列关于Na2CO3和NaHCO3性质的说法错误的是( )
A.热稳定性:NaHCO3<Na2CO3
B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C.相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D.等物质的量浓度溶液的pH:NaHCO3<Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除杂方案错误的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A | CO(g) | CO2(g) | NaOH溶液、浓H2SO4 | 洗气 |
| B | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
| D | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO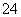 。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如下流程图:
。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如下流程图:
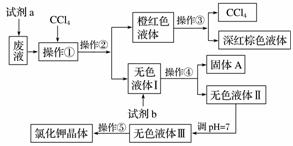
可供试剂a、试剂b(试剂b代表一组试剂)选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液、KMnO4溶液(H+)、稀盐酸。
请根据流程图,回答相关问题:
(1)试剂a应该选用____________。
(2)操作①②③④⑤的名称是__________(填字母)。
A.萃取、过滤、分液、过滤、蒸发结晶
B.萃取、分液、蒸馏、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶
D.萃取、分液、分液、过滤、蒸发结晶
(3)除去无色液体Ⅰ中的Ca2+、Mg2+、SO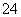 ,选出试剂b所代表的试剂,按滴加顺序依次是________________________(填化学式)。
,选出试剂b所代表的试剂,按滴加顺序依次是________________________(填化学式)。
(4)调节pH的作用是__________________,操作方法是________。
(5)操作⑤中用到的瓷质仪器名称是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是________和________;________和
________________________。
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO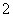 互为等电子体的分子有________、________。
互为等电子体的分子有________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中,含离子键的物质是( ),由极性键形成的极性分子是( ),由极性键形成的非极性分子是( ),由非极性键形成的非极性分子是( )。
A.CO2 B.Br2
C.CaCl2 D.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示:
含氧酸酸性强弱与非羟基氧原子数的关系
| 次氯酸 | 磷酸 | 高氯酸 | |
| 含氧酸 | Cl-OH |
|
|
| 非羟基氧原子数 | 0 | 1 | 3 |
| 酸性 | 弱酸 | 中强酸 | 最强酸 |
(1)亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构简式分别为①________________,②________________。
(2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
①________________________________________________________________________,
②________________________________________________________________________。
(3)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况:________________________________________________________________________,
写出化学方程式:_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
则①与YZ 互为等电子体的分子的化学式:________(任写一种)。
互为等电子体的分子的化学式:________(任写一种)。
②X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
③Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)56号元素位于第________周期________族。
(2)114号元素位于第________周期________族。
(3)25号元素位于第________周期________族。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com