
| 3 |
| 2 |

| c(N2O4) |
| C2(NO2) |


科目:高中化学 来源: 题型:阅读理解
 (2010?崇文区二模)面对全球近期的气候异常,环境问题再次成为焦点.SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径.
(2010?崇文区二模)面对全球近期的气候异常,环境问题再次成为焦点.SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径.| 3 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)面对全球近期的气候异常,环境问题再次成为焦点。SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径。
(1)下列措施中,有利于降低大气中的SO2、NOx、CO2浓度的有 (选填字母)。
a.减少化石燃料的使用,加快开发和利用风能、氢能等新能源
b.使用无磷洗涤用品,减少含磷废物的排放
c.多步行或乘公交车,少用专车或私家车
d.在屋顶安装太阳能热水器为居民提供生活用热水
(2)用甲醇替代作为汽车燃料可降低汽车尾气污染。已知用合成气(CO和H2)合成1 mol液态甲醇吸收热量为131.9 kJ,2H2(g)=CO2(g)+![]() O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式 。
O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式 。
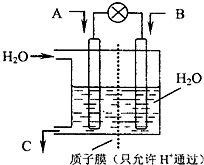
(3)现欲以右图所示装置用电化学原理将CO2、SO2转化为重要化工原料。
①若A为CO2,B为H2,C为CH2OH则通入H2的一极为 极;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为 。
(4)①已知:密闭容器中,17℃、1.01×105Pa条件下,2NO2(g) ![]() N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)=0.030 mol/L,则c(N2O4)= (保留两位有效数字);
N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)=0.030 mol/L,则c(N2O4)= (保留两位有效数字);
②若改变上述体系的某个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04mol/L,c(N2O4)=0.007mol/L,则改变的条件是 。
查看答案和解析>>
科目:高中化学 来源:2010年北京市崇文区高三第二次模拟考试(理综)化学部分 题型:填空题
(14分)面对全球近期的气候异常,环境问题再次成为焦点。SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径。
(1)下列措施中,有利于降低大气中的SO2、NOx、CO2浓度的有 (选填字母)。
a.减少化石燃料的使用,加快开发和利用风能、氢能等新能源
b.使用无磷洗涤用品,减少含磷废物的排放
c.多步行或乘公交车,少用专车或私家车
d.在屋顶安装太阳能热水器为居民提供生活用热水
(2)用甲醇替代作为汽车燃料可降低汽车尾气污染。已知用合成气(CO和H2)合成1 mol液态甲醇吸收热量为131.9 kJ,2H2(g)=CO2(g)+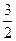 O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式 。
O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式 。
(3)现欲以右图所示装置用电化学原理将CO2、SO2转化为重要化工原料。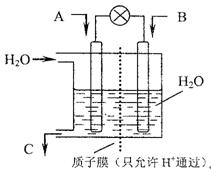
①若A为CO2,B为H2,C为CH2OH 则通入H2的一极为 极;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为 。
(4)①已知:密闭容器中,17℃、1.01×105Pa条件下,2NO2(g)  N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)="0.030" mol/L,则c(N2O4)= (保留两位有效数字);
N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)="0.030" mol/L,则c(N2O4)= (保留两位有效数字);
②若改变上述体系的某个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04mol/L,c(N2O4)=0.007mol/L,则改变的条件是 。
查看答案和解析>>
科目:高中化学 来源:2010年北京市崇文区高三第二次模拟考试(理综)化学部分 题型:填空题
(14分)面对全球近期的气候异常,环境问题再次成为焦点。SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径。
(1)下列措施中,有利于降低大气中的SO2、NOx、CO2浓度的有 (选填字母)。
a.减少化石燃料的使用,加快开发和利用风能、氢能等新能源
b.使用无磷洗涤用品,减少含磷废物的排放
c.多步行或乘公交车,少用专车或私家车
d.在屋顶安装太阳能热水器为居民提供生活用热水
(2)用甲醇替代作为汽车燃料可降低汽车尾气污染。已知用合成气(CO和H2)合成1 mol液态甲醇吸收热量为131.9 kJ,2H2(g)=CO2(g)+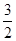 O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式
。
O2(g)2H2O(g)△H=—594.1kJ/mol,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式
。
(3)现欲以右图所示装置用电化学原理将CO2、SO2转化为重要化工原料。
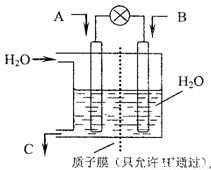
①若A为CO2,B为H2,C为CH2OH 则通入H2的一极为 极;
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为 。
(4)①已知:密闭容器中,17℃、1.01×105Pa条件下,2NO2(g)  N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)=0.030 mol/L,则c(N2O4)=
(保留两位有效数字);
N2O4(g) △H<0的平衡常数K=13.3。当此反应达到平衡时,若c(NO2)=0.030 mol/L,则c(N2O4)=
(保留两位有效数字);
②若改变上述体系的某个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04mol/L,c(N2O4)=0.007mol/L,则改变的条件是 。
查看答案和解析>>
科目:高中化学 来源:0119 同步题 题型:填空题
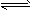 O2+HbCO 实验表明,c(HbCO)即使只有c(HbO2)的1/50,也可造成人的智力损伤。已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2 mol/L,若使c(HbCO)小于c(HbO2)的1/50,则吸入肺部CO的浓度不能超过________mol/L。
O2+HbCO 实验表明,c(HbCO)即使只有c(HbO2)的1/50,也可造成人的智力损伤。已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2 mol/L,若使c(HbCO)小于c(HbO2)的1/50,则吸入肺部CO的浓度不能超过________mol/L。 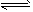 N2(g)+2CO2(g) ΔH=-113 kJ/mol
N2(g)+2CO2(g) ΔH=-113 kJ/mol 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com