
����Ŀ����ͼ��ʾΪԪ�����ڱ��м�Ԫ�ؿ�ͼ��������39.10����ʾ����________��
ij��ѧ��ȤС������ȥ16g�����Ȼ����л��е������Ȼ��ƺ�����þ���ʣ����ʵ�鷽�����£���֪������NaCl���ܽ��Ϊ36g/100g![]() O��
O��

��1����ˮ�ܽ�ʱ���ʺϵ�ȡˮ��Ϊ________
A. 20mL B. 45mL C. 75mL D. 100mL
��2��Ϊ�ӿ��ܽ����ʣ��ɲ�ȡ�ķ�����________��________����д2�֣�
��3�����μ���Ĺ����Լ�Ϊ________��________��________��
��4����ҺA�м����������Ϊ________��������Ҳ�ӹ����������õ��Ȼ��ƵĴ���________��������������û������Ӱ��
��5���������������________������II��������________�����ֲ����ж��õ��IJ���������________��
��6�����õ��Ĺ����Ȼ�����ԭ���������е��Ȼ���������ȣ����________������������������С����������������
��7������A���������εĻ�ѧʽΪ___________��
���𰸡���Ԫ�ص����ԭ������ B ���� ���� �������ƣ����Ȼ����� �Ȼ��������������ƣ� ̼���� ���� û�� ���� �����ᾧ ������ ���� BaSO4��CaCO3��BaCO3
��������
Ԫ�����ڱ��ṩ��ԭ��������ʾijԪ�ص����ԭ��������
��1������16g����ȫ��Ϊ�Ȼ��ƣ�����xgˮ��ǡ���γɱ�����Һ������S/100=����/�ܼ����м��㣬�Ӷ��жϳ����ʵ�ȡˮ����
��2������Ӱ�췴Ӧ���ʵ����ؽ��з�����
��3��þ�������������Ƴ�ȥ��������������Ȼ�����ȥ�������ӡ������ı�������̼���Ƴ�ȥ��
��4����ҺA�к����Ȼ��ơ�ʣ���̼���ƺ��������ƣ�Ҫ�õ��������Ȼ��ƣ��������������ᣬ��ȥ̼������Ӻ����������ӣ����������е��Ȼ����ӷ����ʣ���������ӹ����������õ��Ȼ��ƵĴ���Ӱ�죻
��5�����ݳ������ʵķ��뷽�����з�����
��6�������ڳ�ȥ�Ȼ��ơ�����þ����ʱ�������˹������������ơ�̼���ƣ������ᷴӦ�����Ȼ��ƣ��������õ��Ĺ����Ȼ��Ʊ�ԭ���������е��Ȼ�������Ҫ��
��7��þ�������������Ƴ�ȥ������������þ������������������Ȼ�����ȥ���������ᱵ�����������ӡ������ı�������̼���Ƴ�ȥ������̼��ƺ�̼�ᱵ�������ݴ˷��������ε����ࡣ
����Ԫ�����ڱ��м�Ԫ�ؿ�ͼ��֪��������39.10����ʾ���Ǽ�Ԫ�ص����ԭ��������
�ʴ��ǣ���Ԫ�ص����ԭ��������
��1������16g����ȫ��Ϊ�Ȼ��ƣ�����xgˮ��ǡ���γɱ�����Һ������S/100=����/�ܼ���֪��36g/100g=16g/xg��x=44.4g��ˮ�����Ϊ44.4mL�����Լ�ˮ�ܽ�ʱ���ʺϵ�ȡˮ��Ϊ45mL��
�ʴ�ѡB��
��2��Ϊ�ӿ��ܽ����ʣ��ɲ�ȡ�ķ������ò��������衢����ˮ�ܽ⣻
�ʴ��ǣ����衢���ȣ�
��3��þ�������������Ƴ�ȥ��������������Ȼ�����ȥ�������ӡ������ı�������̼���Ƴ�ȥ��
�ʴ��ǣ��������ƣ����Ȼ��������Ȼ��������������ƣ���̼���ƣ�
��4���������˺���ҺA�к����Ȼ�����ʣ���̼�������������ƣ�Ҫ�õ��������Ȼ��ƣ��������������ᣬ��ȥ̼������Ӻ����������ӣ������е��Ȼ����ӷ�����ˣ���ʹ����ӹ���������Ҳ���Գ�ȥ�������õ��Ȼ��ƵĴ���û��Ӱ�죻
�ʴ��ǣ����û�У�
��5����������Һ���룬���Բ��ù��˷�����������������ǹ��ˣ����Ȼ�����Һ�еõ��Ȼ��ƹ��壬���Բ��������ᾧ������II�������������ᾧ�����˺����������о��õ�������������ʱ����������ת��Һ������ã�������ʱ��������������Һ����ֹҺ��ֲ�������ɱŽ���
�ʴ��ǣ����ˣ������ᾧ����������
��6�������ڳ�ȥ�Ȼ��ơ�����þ����ʱ�������˹����������ơ�̼���ƣ������������Ӻ�ʣ���������ơ�̼���������ᷴӦ�����Ȼ��ƣ��������õ��Ĺ����Ȼ��Ʊ�ԭ���������е��Ȼ�������Ҫ�������
�ʴ��ǣ�����
��7��þ�������������Ƴ�ȥ������������þ������������������Ȼ�����ȥ���������ᱵ�����������ӡ������ı�������̼���Ƴ�ȥ������̼��ƺ�̼�ᱵ���������Ծ������˺���A�к��е���Ϊ�����ᱵ��̼��ƺ�̼�ᱵ����ѧʽΪ��BaSO4��CaCO3��BaCO3��
�ʴ��ǣ�BaSO4��CaCO3��BaCO3��


 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������İ���ͭ����([Cu(NH3)4]SO4��H2O)������ɱ�����ýȾ�����ڼ��Զ�ͭ��Ҳ���������Һ����Ҫ�ɷ֣��ڹ�ҵ����;�㷺�������¸������ڿ����в��ȶ�������ʱ�����ֽ⡣ij��ѧ��ȤС����Cu�ۡ�3mol/L�����ᡢŨ��ˮ��10% NaOH��Һ��95%���Ҵ���Һ��0.500 mol/Lϡ���ᡢ0.500 mol/L��NaOH��Һ���ϳ������İ���ͭ���岢�ⶨ�䴿�ȡ�
I��CuSO4��Һ���Ʊ�
�ٳ�ȡ4gͭ�ۣ���A����������10���Ӳ����Ͻ��裬������ȴ��
�����������м���30mL 3mol/L�����ᣬ��A�й��������������У����Ȳ����Ͻ��衣
�۳��ȹ��˵���ɫ��Һ��
(1)A����������Ϊ________________________________��
(2)ijͬѧ��ʵ������1.5g��ͭ��ʣ�࣬��ͬѧ���Ƶõ�CuSO4��Һ������һ�������м���Ũ�����о�Ĥ���֣���ȴ�����ľ����к��а�ɫ��ĩ���Խ�����ԭ��__________________________________________��
II��������Ʊ�
�������Ʊ���CuSO4��Һ����ͼ��ʾ���в���
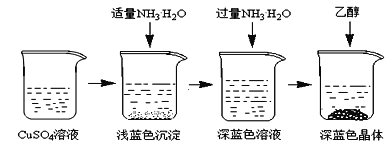
(3)��֪dz��ɫ�����ijɷ�ΪCu2(OH)2SO4����д�����ɴ˳��������ӷ�Ӧ����ʽ___________________��
(4)��������ʱ���ü����Ҵ��ķ�����������Ũ���ᾧ��ԭ����________________________��
III���������IJⶨ
��ȷ��ȡwg������������ˮ�ܽ���ע����ͼ��ʾ������ƿ����Ȼ����μ�������10%NaOH��Һ��ͨ��ˮ����������ƷҺ�еİ�ȫ����������������ˮ��ϴ�����ڱڣ���V1mL0.5mol/L���������Һ��ȫ���ա�ȡ�½���ƿ����0.5mol/L NaOH����Һ�ζ���ʣ��HCl(ѡ�ü�����ָʾ��)�����յ�ʱ����V2mLNaOH��Һ��
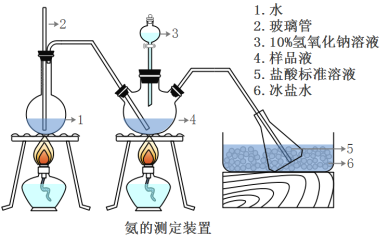
(5)Aװ���г������ܵ�����_________________����Ʒ�а������������ı���ʽ_______��
(6)����ʵ���������ʹ�������ⶨ���ƫ�ߵ�ԭ����____________________��
A���ζ�ʱδ��NaOH����Һ��ϴ�ζ��ܡ�
B������ʱ���ζ�ǰƽ�ӣ��ζ����ӡ�
C���ζ�������ѡ�÷�̪��ָʾ����
D��ȡ�½���ƿǰ��δ������ˮ��ϴ�������ƿ�еĵ�����ڡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���µ�aLHCl(g)����1000gˮ�У��õ��������ܶ�Ϊbg��cm��3�������������ʵ���Ũ���ǣ� ��
A. ![]() mol��L��1B.
mol��L��1B. ![]() mol��L��1
mol��L��1
C. ![]() mol��L��1D.
mol��L��1D. ![]() mol��L��1
mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��XԪ������������Ӧ��ˮ����ΪH3XO4��������Ӧ����̬�⻯��Ϊ( )
A. HXB. H2XC. XH3D. XH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ���������ֵ������˵����ȷ����
A. �ں�CO32-����ΪNA��Na2CO3��Һ�У�Na+����Ϊ2NA
B. ��״���£�2.24 L����ͱ�ϩ�Ļ�����к���ԭ����ĿΪ0.6NA
C. ��0.1 mol H2��0.2 mol I2(g)�����ܱ������г�ַ�Ӧ�����ɵ�H-I����ĿΪ0.2NA
D. �����£����1 L�ľ���ʳ��ˮ��һ��ʱ�������ҺpHΪ11�����������ͨ�����ߵĵ�����ĿΪ0.002NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ӱ�컯ѧ��Ӧ���ʵ����غܶ࣬ij��ѧС����ʵ��ķ�������̽����
I��̽���һ��
��ѡҩƷ����Ƭ��пƬ��0.5mol/LH2SO4��1.5mol/LH2SO4��18.4mol/LH2SO4
��ͬѧ�о���ʵ�鱨��
ʵ�鲽�� | ���� | ���� |
�ٷֱ�ȡ�������1.5mol/L����������֧�Թ��У� ��_____________________�� | ��Ӧ���ʣ� п>�� | ����������Խ���ã���Ӧ����Խ�� |
(1)��ͬѧʵ�鱨���е�ʵ�鲽���Ϊ__________________________________��
(2)��ͬѧ��ʵ��Ŀ����_______________________________��Ҫ�ó���ȷ��ʵ����ۣ�������Ƶ�ʵ��������__________________��
��ͬѧΪ�˶����о�Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬������ͼ��ʾװ�ý���ʵ�飺

(3)��ͬѧ��ʵ������Ҫ�ⶨ��������_________________________��
(4)��ͬѧ����ѡ��___________mol/L������ɸ�ʵ�飬������_________________��
II��̽�������
��ѡҩƷ��0.1mol/LNa2S2O3��Һ��0.2mol/LNa2S2O3��Һ��0.1mol/LH2SO4��Һ��0.2mol/LH2SO4��Һ��
��֪��Na2S2O3��H2SO4��Na2SO4��S����SO2����H2O
ʵ�� ��� | Na2S2O3���� | H2SO4���� | �¶ȣ����� |
�� | 0.1mol/L5mL | 0.1mol/L5mL | 10 |
�� | 0.2mol/L5mL | 0.2mol/L5mL | 25 |
�� | 0.1mol/L5mL | 0.1mol/L5mL | 25 |
�� | 0.1mol/L5mL | 0.1mol/L5mL | 40 |
(1)����̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬��ѡ��ʵ������___________��
(2)����̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬��ѡ��ʵ������___________��
(3)�ڸ�ʵ������У���Ҫ�۲�ͼ�¼________________�����Ƚϻ�ѧ��Ӧ���ʵĿ�����
(4)Na2S2O3�ڼ�����Һ�пɱ�I2����ΪNa2SO4��д���÷�Ӧ�����ӷ���ʽ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ�ĵ���,�Dz������Ļ�����Ʒ֮һ����ϳ�ԭ��Ϊ: N2��g��+3H2��g��![]() 2NH3��g������H= - 92.4 kJ��mol-1.
2NH3��g������H= - 92.4 kJ��mol-1.
I.���ܱ������У�Ͷ��1mol N2��3 mol H2�ڴ��������·�����Ӧ:
(1)��÷�Ӧ�ų�������_________92.4kJ������С����������������������������
(2)����Ӧ�ﵽƽ��ʱ��N2��H2��Ũ�ȱ���_________��N2��H2��ת���ʱ���___________��
(3)����ƽ����ϵ���¶�(�����������)����������ƽ����Է�������____��(���������������С������������)
(4)���ﵽƽ��ʱ�����������������ѹǿ���䣬ƽ�⽫____(����������������������������)�ƶ���
II.�÷�Ӧ��һ�ܱ������з�������ͼ��ijһʱ��η�Ӧ�����뷴Ӧ���̵Ĺ�ϵ����ͼ��

(1)t1ʱ�̣���ϵ�з����仯��������_______ ��
A������ѹǿB�������¶�C����СѹǿD�������¶� E������������
(2)����ʱ����У����İٷֺ�����ߵ���_______��
A��0��t1 B��t2��t3 C��t3��t4 D��t4��t5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ������ȷ����
A. (NH4)2 Fe(SO4)2 �ܽ���ˮ��(NH4)2 Fe(SO4)2 ![]() 2NH4+ + Fe2 + + 2SO42��
2NH4+ + Fe2 + + 2SO42��
B. Al(OH)3��ˮ�еĵ��룺Al(OH)3 ![]() Al3 ++3OH��
Al3 ++3OH��
C. H3PO4�ܽ���ˮ��H3PO4 ![]() 3H+ + PO43��
3H+ + PO43��
D. NaHSO3��ˮ�еĵ��룺HSO3�� + H3O+![]() SO32��+ H2O
SO32��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ����
A. ��25�桢101 kPaʱ��2 gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ���ȵ��Ȼ�ѧ����ʽΪ��2H2(g)+O2(g)![]() 2H2O(l)����H=��285.8kJ��mol-1
2H2O(l)����H=��285.8kJ��mol-1
B. CO(g)��ȼ������283.0 kJ/mol����2CO2(g)![]() 2CO(g)+O2(g)����H=+283.0 kJ/mol
2CO(g)+O2(g)����H=+283.0 kJ/mol
C. ��ϡ��Һ�У�H+(aq)+OH��(aq)= H2O(l)����H =��57.3 kJ��mol��1��������0.5 mol H2SO4��ϡ������1 mol NaOH�����ϣ��ų�����������57.3 kJ
D. ��֪C(ʯī,s) ![]() C(���ʯ,s)����H��+1.9 kJ/mol������ʯ��ʯī�ȶ�
C(���ʯ,s)����H��+1.9 kJ/mol������ʯ��ʯī�ȶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com