
| A、氧化性:H2SeO4>C12>H2SO3 |
| B、酸性:H2SO4>H2SeO4 |
| C、析出l mol硒需要消耗标准状况下22.4L SO2 |
| D、硒酸转化为亚硒酸的反应中氧化产物为Cl2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeSO4溶液存放在加有少量铁粉的试剂瓶中 |
| B、金属钠着火燃烧时,用泡沫灭火器灭火 |
| C、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| D、NaOH溶液装在带玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将SO2通入BaCl2溶液中至饱和,无沉淀产生;再通人Cl2产生沉淀 |
| B、向AlC13溶液中加氨水,产生白色沉淀;再加入过量氨水,沉淀消失 |
| C、在稀硫酸中加入铜粉,铜粉不溶解;再加入NaNO3固体,铜粉溶解 |
| D、纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量CuSO4固体,速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向AlCl3溶液中加过量的NaOH溶液 |
| B、向NaAlO2溶液中加过量的盐酸 |
| C、向AlCl3溶液中通入过量的CO2 |
| D、向NaAlO2溶液中通入过量的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
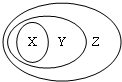 用图表示的一些物质或概念间的从属关系中不正确的是( )
用图表示的一些物质或概念间的从属关系中不正确的是( )| X | Y | Z | |
| A | 氧化物 | 化合物 | 纯净物 |
| B | 电解质 | 盐 | 化合物 |
| C | 胶体 | 分散系 | 混合物 |
| D | 酸性氧化物 | 非金属氧化物 | 氧化物 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com