
向只含有Fe3+、Cu2+、H+各0.1 mol及a mol SO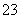 的某溶液中(只来源于水电离的离子不考虑)加入足量锌粉,搅拌使其充分反应,下列说法中正确的是( )
的某溶液中(只来源于水电离的离子不考虑)加入足量锌粉,搅拌使其充分反应,下列说法中正确的是( )
A.当消耗0.1 mol Zn时,得到的还原产物为0.1 mol
B.当溶液中不再产生气泡时,溶液中大量存在的阳离子只有Zn2+
C.最后生成的单质为Fe
D.反应结束时,可得到0.25 mol ZnSO4
解析:本题考查了离子反应和氧化还原反应,意在考查考生对金属活动性顺序表的理解及应用能力。根据金属活动性顺序表知,当消耗0.05 mol Zn时,Fe3+被还原,生成0.1 mol Fe2+,再消耗0.05 mol Zn时,生成0.05 mol Cu,即消耗0.1 mol Zn时,得到的还原产物为0.15 mol,A项错误;加入足量锌,发生反应的顺序是Fe3+、Cu2+、H+、Fe2+,故不再产生气泡时,溶液中除存在Zn2+外,还存在Fe2+,B项错误,C项正确;根据得失电子守恒可知,0.1 mol Fe3+最终转化为Fe,需要锌0.15 mol,0.1 mol Cu2+转化为Cu需要锌0.1 mol,0.1 mol H+转化为氢气需要锌0.05 mol,共需要锌0.3 mol,即反应结束时硫酸锌为0.3 mol,D项错误。
答案:C


科目:高中化学 来源: 题型:
已知同温同压下,下列反应的焓变和平衡常数分别表示为
(1)2SO2(g)+O2(g)2SO3(g)
ΔH1=-197 kJ·mol-1 K1=a
(2)2NO(g)+O2(g)2NO2(g)
ΔH2=-144 kJ·mol-1 K2=b
(3)NO2(g)+SO2(g)SO3(g)+NO(g)
ΔH3=-m kJ·mol-1 K3 =c
下列说法正确的是( )
A.m=53 c2=a/b B.m=-26.5 2c=a-b
C.m=-170.5 2c=a-b D.m=26.5 c2=a/b
查看答案和解析>>
科目:高中化学 来源: 题型:
NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:____________________。
(3)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:____________________________________________________________
________________________________________________________________________。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO。原因是_______________________________,
元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作、现象和原因解释不合理的是( )
| 选项 | 实验操作 | 实验现象 | 原因解释 |
| A | 将一片较薄的铝片放在酒精灯火焰上灼烧 | 铝片慢慢熔化呈液滴状 | 铝表面的氧化膜致密且熔点很高,阻碍铝与氧气的接触,同时铝的熔点较低,熔化了 |
| B | 将等表面积的镁条、铝片(均除去氧化膜)分别放入装有等浓度、等体积盐酸的两支试管中 | 都产生气泡,镁条表面产生气泡更快 | 镁的金属性比铝的金属性强,镁更易失去电子,所以反应更快 |
| C | 在打磨过的铁片上先滴一滴饱和食盐水,再滴一滴酚酞 | 液滴的外圈先出现红色 | 铁片不纯含有碳元素,铁、碳与食盐水形成原电池,溶液外圈发生吸氧腐蚀,导致c(OH-)增 大,溶液呈碱性 |
| D | 取少量淀粉和稀硫酸,加热几分钟,冷却后加入新制氢氧化铜,加热至沸腾 | 未见砖红色沉淀生成 | 淀粉水解后没有葡萄糖生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在氧气中灼烧硫和铁组成的化合物0.44 g,使其中的硫全部转化为二氧化硫,把这些二氧化硫全部氧化成硫酸。这些硫酸可以用20 mL 0.5 mol/L氢氧化钠完全中和。则原化合物中硫的质量分数约为( )
A.18% B.46%
C.53% D.36%
查看答案和解析>>
科目:高中化学 来源: 题型:
研究性学习小组对某硫酸亚铁晶体(FeSO4·xH2O)热分解研究,该小组同学称取a g硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B质量测出x的值。

(1)装置B中硫酸铜粉末变蓝,质量增加12.6 g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中还有________________。
(2)实验中要持续通入氮气,否则测出的x会_________ (填“偏大”、“偏小”或“不变”)。
(3)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体Fe2O3。
(4)从理论上分析得出硫酸亚铁分解还生成另一物质SO3,写出FeSO4分解的化学方程式________________。
(5)装置D球形干燥管的作用________________。
(6)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4·xH2O)进行热分解,获得相关数据,绘制成固体质量-分解温度的关系图如图2,根据图2中有关数据,可计算出FeSO4·xH2O中的x=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 室温下,测定等浓度的CH3COOH溶液和盐酸的pH | 比较两种酸的酸性强弱 |
| B | CH3CH2Br 中加入NaOH溶液加热充分反应,取上层水溶液加入AgNO3溶液 | 检验CH3CH2Br中的溴原子 |
| C | 向25ml沸水中滴加4—5滴饱和FeCl3溶液,加热至有红褐色沉淀产生 | 制备Fe(OH)3胶体 |
| D | 在某溶液中先加入HNO3溶液,再加入Ba(NO3)2溶液 | 检验溶液中是否存在SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)钢铁在潮湿的空气中发生吸氧腐蚀的正极反应式为________________________。
(2)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,Y可溶于过量盐酸,形成黄绿色的溶液,写出Y与盐酸反应的化学方程式:_____________________________________________________________________。
(3)某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl2·2H2O的工艺流程如下:
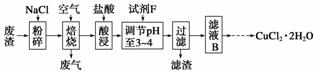
已知:a.Fe(OH)2、Fe(OH)3、Cu(OH)2沉淀完全时的pH值分别为9.7、3.2、6.4;
b.高温煅烧时CuS发生的主要反应为CuS+NaCl+O2—→CuCl2+Na2SO4(未配平)。
试回答下列问题:
①试剂F应选用________(填编号)。
A.Cl2 B.NaClO C.HNO3 D.浓硫酸
理由是_______________________________________________________________。
②为了获得CuCl2·2H2O晶体,对滤液B进行的操作是蒸发浓缩,趁热过滤,滤液经冷却结晶,过滤得到产品。分析有关物质的溶解度曲线(如图),“趁热过滤”得到的固体是____________。
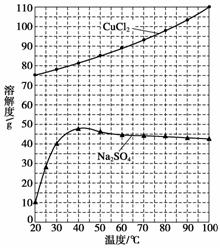
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的
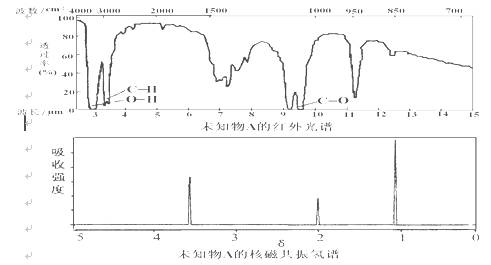
A.由红光外谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com