
A、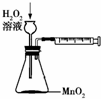 用以定量测定化学反应速率 |
B、 为用已知浓度的氢氧化钠溶液测定未知浓度盐酸的实验 |
C、 可以检查装置的气密性 |
D、 为实验室制取少量CO2的发生装置 |


科目:高中化学 来源: 题型:
 工、农业废水以及生活污水中浓度较高的NO3-会造成氮污染.工业上处理水体中NO3-的一种方法是零价铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.
工、农业废水以及生活污水中浓度较高的NO3-会造成氮污染.工业上处理水体中NO3-的一种方法是零价铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.查看答案和解析>>
科目:高中化学 来源: 题型:
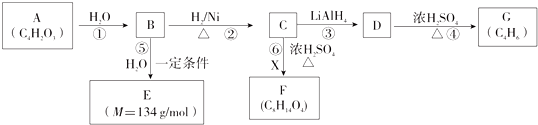

| H2O |
| LiAlH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)=10-13mol/L的溶液中:NO3-、SO42-、K+、Na+ |
| B、澄清石灰水中:Na+、K+、CH3COO -、HCO3- |
| C、铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- |
| D、空气中:SO2、NO、N2、NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A
A| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸保存在棕色试剂瓶中 |
| B、金属钠通常保存在煤油里,不能保存在四氯化碳中 |
| C、烧碱溶液保存在带玻璃塞的磨口试剂瓶中 |
| D、配置一定物质的量浓度的氯化钠溶液时,要将氯化钠固体放在滤纸上称量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4、C3H6 |
| B、CH4、C2H4 |
| C、C2H4、C3H8 |
| D、C2H6、C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | Z | |
| ① | NaOH溶液 | Al | 稀硫酸 |
| ② | KOH溶液 | Br2 | Na2SO3溶液 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A、只有①③④ |
| B、只有①②④ |
| C、只有①②③ |
| D、①②③④皆可 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com