
【题目】下列各溶液中,Na+浓度最大的是
A.0.8L0.4mol/L的NaOH溶液B.0.2L0.15mol/L的Na3PO4溶液
C.1L0.3mol/L的NaCl溶液D.4L0.5mol/L的NaCl溶液
科目:高中化学 来源: 题型:
【题目】下列说法正确的( )
A. 合金的熔点比其组成成分金属的熔点高
B. SO2具有漂白性能使紫色石蕊试液先变红后褪色
C. 因Fe、Al常温下与浓硝酸反应,故不能用Fe或Al制器皿盛放浓硝酸
D. 液溴易挥发且密度大于水,保存时,用水封法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由石油裂解产物乙烯制取HOCH2COOH,需要经历的反应类型有( )
A.氧化——氧化——取代——水解
B.加成——水解——氧化——氧化
C.氧化——取代——氧化——水解
D.水解——氧化——氧化——取代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验. 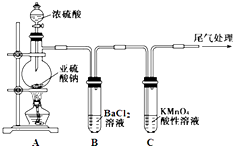
已知:Na2SO3+H2SO4(浓) ![]() Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是 .
(2)实验过程中,C中的现象是 , 说明SO2具有性.
(3)实验过程中,观察到装置B中出现了明显的白色沉淀.为探究该白色沉淀的成分,该小组同学进行了如下实验: ![]()
根据实验事实判断该白色沉淀的成分是(填化学式),产生该白色沉淀的原因可能是(填字母编号).
a.BaSO3既不溶于水也不溶于酸 b.BaCl2溶液中可能溶解有氧气
c.BaCl2溶液中可能混有NaOH d.由A制得的SO2气体中可能混有氧气
(4)如果将装置A中的浓H2SO4换作浓HNO3 , 对此实验是否有影响并明理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A | B | C | D |
|
|
|
|
放电闪电时会发生反应:N2+O2═2NO | 利用丁达尔效应证明烧杯中的分散系是胶体 | 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 | 加热时熔化的铝不滴落,证明Al2O3的熔点比Al高 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO的应用和治理问题属于当今社会的热点问题.
(1)汽车尾气中CO的治理,常用四氧化三钴(Co3O4)纳米棒的作催化剂,低温下与O2反应生成CO2 . 下列说法中正确的是(不定项选择)
A.该反应是分解反应
B.反应前后Co3O4化学性质不改变
C.反应前后碳元素的化合价不变
D.该反应的△H<0
(2)光气(COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)COCl2(g)制备.左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线.回答下列问题: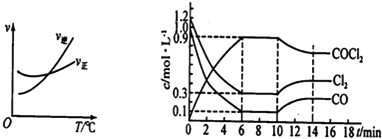
①0~6min内,反应的平均速率v(Cl2)=;
②若保持温度不变,在第8min加入体系中的三种物质各1mol,则平衡移动(填“向正反应方向”、“向逆反应方向”或“不”);
③若将初始投料浓度变为c(Cl2)=0.8mol/L、c(CO)=0.6mol/L、c(COCl2)=mol/L,保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同;
④该反应的平衡常数的表达式为K= , 随温度升高,该反应平衡常数变化的趋势为(填“增大”、“减小”或“不变”),原因为⑤比较第8min反应温度T(8)与第15min反应温度T(15)的高低:T(8)T(15)(填“<”、“>”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)质量之比为7:6的两种气体CO和NO,分子数之比为;氧原子数之比为;相同条件下的体积之比为 .
(2)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mgmol﹣1 . 若阿伏加德罗常数用NA表示,则:①该气体的物质的量为mol.
②该气体所含原子总数为个.
③该气体在标准状况下的体积为L.
④该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 .
⑤该气体溶于水后形成VL溶液,其溶液的物质的量浓度为molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数,下列说法正确的是( )
A.1molFe与足量的Cl2反应转移的电子数为2NA
B.标准状况下,22.4L水中含有的水分子数为NA
C.常温、常压下,22gCO2中含有的氧原子数为NA
D.0.11mol/LCaCl2溶液中含氧离子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究工业废弃物的处理和防治具有重要的意义.
(1)利用反应CH4+2NO2 ![]() N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是 , 当消耗CH4的体积是11.2L(标准状况下)时,理论上可处理molNO2 .
N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是 , 当消耗CH4的体积是11.2L(标准状况下)时,理论上可处理molNO2 .
(2)治理汽车尾气中CO和NO的一种方法是:在汽车排气管中安装一个催化转化装置,该装置能将CO和NO转化为参与大气循环的无毒气体.该反应的化学方程式为
(3)某工厂排放的工业废水中可能含有Fe3+、Al3+、Cu2+ , 为了减少环境污染,变废为宝,利用废铁屑制得Fe2O3、Al2O3和金属Cu,过程如下.
①固体A的成分是 . (填化学式)
②溶液B中的阳离子有 .
③D与过量H溶液反应生成E的离子方程式是 .
④溶液E焰色呈黄色,试剂H是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com