
【题目】钼及其合金在冶金、环保和航天等方面有着广泛的应用。
(1)Mo可被发烟硝酸及氢氟酸氧化为MoO2F2和MoOF4(少量),硝酸本身被还原为NO2,则该反应中氧化剂与还原剂的物质的量之比为_________
(2)已知:2Mo(s)+3O2(g)==2MoO3(s)△H1 ;
2MoS2(s)+ 7O2(g)= 2MoO3(s)+4SO2(g)△H2 ;
MoS2(s)+2O2(g)=Mo(s)+2SO2 (g)△H3
则△H3=_______(用含△Hl、△H2的代数式表示)。
(3)电氧化法提纯钼的原理:将辉钼矿(MoS2)放入装有食盐水的电解槽中,用惰性电极电解,MoS2被氧化为MoO42-和SO42-。
① 辉钼矿应放入电解槽的__________(填“阴极区”或“阳极区”)。
② 阴极的电极反应式为______________。
(4)碳酸钠作固硫剂并用氢还原辉钼矿的原理为MoOS2(s)+4H2(g) +2Na2CO3(s)![]() MO(s)+2CO(g)+4H2O(g)+2Na2S(s)△H,实验测得平衡时的有关变化曲线如图所示。
MO(s)+2CO(g)+4H2O(g)+2Na2S(s)△H,实验测得平衡时的有关变化曲线如图所示。
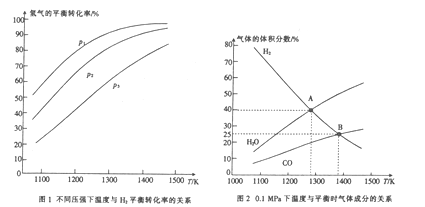
① 由图l可知,该反应△H___(填“>”或“<”)0,p1、p2、p3由大到小的顺序为____。
② 由图2可知,A点时H2的平衡转化率为____。
③ B点对应的平衡常数K=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(MPa)2 。
【答案】 6:1 1/2△H2-1/2△H1 阳极区 2H2O+2e-=H2↑+2OH-(或2H++2e-=H2↑) > p3>p2>p1 50% 0.01
【解析】(1) Mo可被发烟硝酸及氢氟酸氧化为MoO2F2和MoOF4(少量),硝酸本身被还原为NO2,Mo从0价升高为+6价,N元素从+5价降为+4价,根据电子转移守恒,则该反应中氧化剂与还原剂的物质的量之比为6:1;
(2)已知:①2Mo(s)+3O2(g)==2MoO3(s)△H1;②2MoS2(s)+ 7O2(g)= 2MoO3(s)+4SO2(g)△H2 ;根据盖斯定律,MoS2(s)+2O2(g)=Mo(s)+2SO2 (g)可由②×![]() -①×
-①×![]() 得,则△H3=(△H2 )×
得,则△H3=(△H2 )×![]() -(△H1)×
-(△H1)×![]() =
=![]() (△H2 -△H1);
(△H2 -△H1);
(3)① MoS2被氧化为MoO42-和SO42-,电解池的阳极区发生氧化反应,则辉钼矿应放入电解槽的阳极区;
② 阴极发生还原反应,是水电离的H+得电子还原为氢气,电极反应式为 2H2O+2e-=H2↑+2OH-(或2H++2e-=H2↑);
(4)① 由图l可知,氢气的转化率随温度升高而升高,说明温度升高平衡正向移动,即正反应为吸热反应,即该反应△H<0,在恒温条件下,增大压强平衡逆向移动,氢气的转化率应降低,则由图示可知p1、p2、p3由大到小的顺序为p3>p2>p1 ;
② MoOS2(s)+4H2(g)+2Na2CO3(s)![]() MO(s)+2CO(g)+4H2O(g)+2Na2S(s)
MO(s)+2CO(g)+4H2O(g)+2Na2S(s)
设A点时混合气体的总物质的量为1mol,则H2的物质的量为0.4mol,H2O(g)的物质的量为0.4mol,则变化的H2的物质的量为0.4mol,A点时H2的平衡转化率为![]() ×100%=50%;
×100%=50%;
③B点时H2、CO的体积分数均为25%=0.25,则H2O(g)的体积分数为0.5,B点对应的平衡常数K=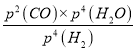 =
=![]() =0.01。
=0.01。


科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
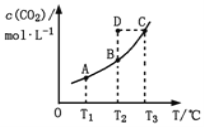
A. 反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的 ΔH>0
CO2(g)+H2(g)的 ΔH>0
B. 在T2时,若反应处于状态D,则一定有ν正<ν逆
C. 平衡状态A与C相比,平衡状态A的c(CO)小
D. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.煤、石油、天然气均为化石燃料,它们属于可再生资源
B.大自然利用太阳能最成功的是植物的光合作用
C.石油的分馏、催化裂化、裂解等石油加工方法,其目的均为得到更多的汽油
D.化肥的大量使用不会造成环境污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)下列分离和提纯物质的方法错误的是( )
物质 | 杂志 | 试剂或用品 | 主要操作 | |
A | 淀粉 | 碘化钾 | 半透膜 | 渗析 |
B | Fe(NO3)2 | Ba(NO3)2 | 硫酸 | 过滤 |
C | Fe | I2 | / | 加热 |
D | 溴 | 四氧化碳 | 蒸馏装置 | 蒸馏 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题。
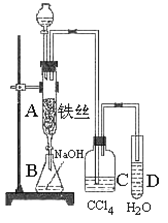
(1)写出A中发生的有机反应的化学方程式_____________________;
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是____________,然后用_______________仪器分离出溴苯(仍含有少量苯);
(3)反应完毕后,向试管D中滴加AgNO3溶液有_______(填现象)生成,此现象说明这种获得溴苯的反应属于________反应(填有机反应类型)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列不发生反应的一组物质是( ) ①铜与浓硫酸 ②二氧化硅与NaOH溶液 ③铜与浓硝酸 ④石英与水⑤铁与液氯 ⑥一氧化氮与氧气 ⑦硅与氧气 ⑧H2S与SO2 .
A.①②③⑥
B.②③⑥⑧
C.①④⑤⑦
D.①②③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,下列反应可制取K2FeO4:
2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O。下列说法不正确的是( )
A.该反应是置换反应 B.氢氧化铁胶体可以净水
C.该反应中铁元素化合价升高 D.高铁酸钾具有很强的氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为( )
A. -1780kJ/mol B. -1220 kJ/mol
C. -450 kJ/mol D. +430 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com