
分析 (1)Fe(OH)2较Cu(OH)2的溶解度小,为除去Fe2+,应转化为溶解度更小的Fe(OH)3;
(2)调整溶液pH值在3~4之间,可加入能与酸反应的物质,注意不能引入新杂质;
(3)三氯化锑水解呈酸性,生成Sb(OH)3和盐酸,配制溶液时应注意抑制水解.
解答 解:(1)Fe(OH)2较Cu(OH)2的溶解度小,为除去Fe2+,应转化为溶解度更小的Fe(OH)3,可加入适当的氧化剂氧化,使之生成Fe3+,
故答案为:加入适当的氧化剂氧化,使之生成Fe3+;
(2)调整溶液pH值在3~4之间,可加入能与酸反应的物质,注意不能引入新杂质,可加入CuO或Cu(OH)2或CuCO3等,故答案为:CuO或Cu(OH)2或CuCO3等;
(3)三氯化锑水解呈酸性,溶液pH<7,生成Sb(OH)3和盐酸,方程式为SbCl3+3H2O=Sb(OH)3↓+3HCl,配制溶液时应注意抑制水解,可将SbCl3溶解在浓HCl中,再加水稀释至所需浓度,
故答案为:小于;SbCl3+3H2O=Sb(OH)3↓+3HCl;将SbCl3溶解在浓HCl中,再加水稀释至所需浓度.
点评 本题考查制备实验方案的设计,为高频考点,把握制备流程及发生的反应、混合物分离提纯、盐类水解等为解答的关键,综合考查反应原理及实验能力,注意表格数据应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
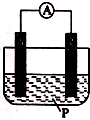 如图所示装置中,可观察到电流表指针偏转;M棒变粗,N棒变细,由此判断下表所列M、N、P物质,其中可以成立的是 ( )
如图所示装置中,可观察到电流表指针偏转;M棒变粗,N棒变细,由此判断下表所列M、N、P物质,其中可以成立的是 ( )| 选项 | M | N | P |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 锌 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
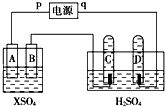 如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡,试回答:
如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
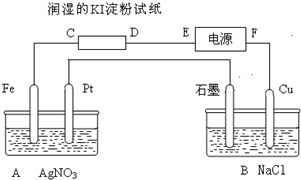 有电解装置如图所示.图中A装置盛1L 2mol/L AgNO3溶液.通电后,润湿的淀粉KI试纸的C端变蓝色,电解一段时间后试回答:
有电解装置如图所示.图中A装置盛1L 2mol/L AgNO3溶液.通电后,润湿的淀粉KI试纸的C端变蓝色,电解一段时间后试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质的最外层电子数都是7 | |
| B. | 卤素单质与H2化合的容易程度为F2<Cl2<Br2<I2 | |
| C. | 卤素单质与H2化合的产物由上至下稳定性减弱,其水溶液的酸性增强 | |
| D. | 从F到I,元素非金属性依次减弱,则其最高价氧化物的水化物的酸依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数 | B. | 质量数 | C. | 中子数 | D. | 电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com