
| ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0 | |
| 2 | ¢Ü | ¢Ż | ||||||
| 3 | ¢Ł | ¢Ś | ¢Ū | ¢Ž | ¢ß | ¢ą |
| ŹµŃé²½Öč | ŹµŃéĻÖĻó |
| A”¢½«Ņ»Š”æ鵄֏¢Ł·ÅČėµĪÓŠ·ÓĢŖČÜŅŗ µÄĄäĖ®ÖŠ | ¾ēĮŅ·“Ó¦£¬¢Łø”ÓŚĖ®ĆęÉĻ£¬ČŪ³ÉŠ”Ēņ£¬ĖÄ“¦ÓĪ¶Æ£¬·¢³ö”°Ė»Ė»”±Éł£¬ĖęÖ®ĻūŹ§£¬ČÜŅŗ±ä³ÉŗģÉ« |
| B”¢½«µ„ÖŹ¢ŚĶ¶ČėĄäĖ®ÖŠ£¬¹Ū²ģĻÖĻó£¬ ŌŁ½«Ė®¼ÓČČ | æŖŹ¼ĪŽĻÖĻ󣬼ÓČČŗóÓŠĘųĢå²śÉś |
| C”¢½«µ„ÖŹ¢ŚĶ¶ČėĻ”ŃĪĖįÖŠ | ŃøĖŁ²śÉś“óĮæĪŽÉ«ĘųĢå |
| D”¢½«µ„ÖŹ¢ŪĶ¶ČėĻ”ŃĪĖįÖŠ | ·“Ó¦²»Ź®·Ö¾ēĮŅ£¬²śÉśĪŽÉ«ĘųĢå |
·ÖĪö ÓÉŌŖĖŲŌŚÖÜĘŚ±ķµÄĪ»ÖĆæÉÖŖ£¬¢Ł”«¢ą·Ö±šĪŖNa”¢Mg”¢Al”¢C”¢N”¢S”¢Cl”¢Ar£¬
£Ø1£©NaµÄ½šŹōŠŌ×īĒ棬ArµÄŠŌÖŹ×īĪČ¶Ø£»
£Ø2£©ÓÉ¢Ł”¢¢ÜÓėŃõČżÖÖŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļ£¬ĘäĖ®ČÜŅŗĻ“µÓÓĶĪŪĪļĘ·Ź±£¬ÓėĖ®½āÓŠ¹Ų£»
£Ø3£©½šøÕŹÆÓėŹÆÄ«¾łĪŖCµÄµ„ÖŹ£»
£Ø4£©¢ŁµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĪŖNaOH£¬¢ŻµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĪŖĻõĖį£¬¶žÕß·“Ӧɜ³ÉĻõĖįÄĘŗĶĖ®£»
£Ø5£©½šŹōÓėĖ®ÓėĖįµÄ·“Ó¦Ō½¾ēĮŅ£¬Ōņ½šŹōŠŌŌ½Ē棻±Č½Ļ¢ŽÓė¢ßµÄµ„ÖŹµÄ»īĘĆŠŌ£¬æÉĄūÓƵ„ÖŹÖ®¼äµÄÖĆ»»·“Ó¦ĖµĆ÷£®
½ā“š ½ā£ŗÓÉŌŖĖŲŌŚÖÜĘŚ±ķµÄĪ»ÖĆæÉÖŖ£¬¢Ł”«¢ą·Ö±šĪŖNa”¢Mg”¢Al”¢C”¢N”¢S”¢Cl”¢Ar£¬
£Ø1£©8ÖÖŌŖĖŲÖŠ£¬½šŹōŠŌ×īĒæµÄŹĒNa£¬»ÆѧŠŌÖŹ×ī²»»īĘƵďĒAr£¬¹Ź“š°øĪŖ£ŗNa£»Ar£»
£Ø2£©ÓĆČȵÄĖ®ČÜŅŗČ„ÓĶĪŪµÄŠ§¹ū±Č½ĻŗĆ”±µÄŌŅņŹĒ¼ÓČČ“Ł½ų“æ¼īĖ®½ā£¬Ź¹OH-ÅضČŌö“ó£¬ŌöĒæĮĖČ„ÓĶĪŪµÄÄÜĮ¦£¬
¹Ź“š°øĪŖ£ŗ¼ÓČČ“Ł½ų“æ¼īĖ®½ā£¬Ź¹OH-ÅضČŌö“ó£¬ŌöĒæĮĖČ„ÓĶĪŪµÄÄÜĮ¦£»
£Ø3£©Ģ¼µÄĮ½ÖÖĶ¬ĖŲŅģŠĪĢåµÄĆū³Ę£ŗ½šøÕŹÆ”¢ŹÆÄ«£Ø»ņĢ¼-60£©£¬¹Ź“š°øĪŖ£ŗ½šøÕŹÆ£»ŹÆÄ«£»
£Ø4£©¢ŁµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĪŖNaOH£¬¢ŻµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĪŖĻõĖį£¬¶žÕß·“Ӧɜ³ÉĻõĖįÄĘŗĶĖ®£¬·“Ó¦ĪŖNaOH+HNO3=NaNO3+H2O£¬
¹Ź“š°øĪŖ£ŗNaOH+HNO3=NaNO3+H2O£»
£Ø5£©ÓÉŹµŃé²½ÖčŗĶĻÖĻóæÉÖŖ£¬½šŹōÓėĖ®ÓėĖįµÄ·“Ó¦Ō½¾ēĮŅ£¬Ōņ½šŹōŠŌŌ½Ē棬ŌņŹµŃé½įĀŪĪŖ½šŹōŠŌ£ŗNa£¾Mg£¾Al£»Čō±Č½Ļ¢ŽÓė¢ßµÄµ„ÖŹµÄ»īĘĆŠŌ£¬ŹµŃé·½°øĪŖĻņNa2S»ņH2SČÜŅŗÖŠĶØČėCl2£¬Čō¹Ū²ģµ½ÓŠµ»ĘÉ«»ģ×Ē£¬Ōņ»īĘĆŠŌCl2ĒæÓŚS£Ø»ņHCl±ČH2SĪČ¶Ø£©£¬
¹Ź“š°øĪŖ£ŗ½šŹōŠŌ£ŗNa£¾Mg£¾Al£»ĻņNa2S»ņH2SČÜŅŗÖŠĶØČėCl2£¬Čō¹Ū²ģµ½ÓŠµ»ĘÉ«»ģ×Ē£¬Ōņ»īĘĆŠŌCl2ĒæÓŚS£Ø»ņHCl±ČH2SĪČ¶Ø£©£®
µćĘĄ ±¾Ģāæ¼²éŹµŃé·½°øµÄÉč¼Ę¼°Ī»ÖĆ”¢½į¹¹ÓėŠŌÖŹµÄ¹ŲĻµ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲµÄĪ»ÖĆ”¢ŠŌÖŹ”¢ŌŖĖŲ»ÆŗĻĪļÖŖŹ¶¼°ŌŖĖŲÖÜĘŚĀÉĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā¹ęĀÉŠŌÖŖŹ¶µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø
æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø ĆūĢāѵĮ·ĻµĮŠ“š°ø
ĆūĢāѵĮ·ĻµĮŠ“š°ø ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā

| A£® | øĆĒāŃõ»ÆÄĘČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0.1 mol/L | |
| B£® | ŌŚbµć£¬c £ØNa+£©ØTc£ØCH3COO-£© | |
| C£® | ŌŚdµć£¬ČÜŅŗÖŠĖłÓŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖc £ØCH3COO-£©£¾c £ØH+ £©£¾c £ØNa+£©£¾c £ØOH-£© | |
| D£® | ĒāŃõ»ÆÄĘČÜŅŗÓė“×ĖįČÜŅŗĒ”ŗĆĶźČ«·“Ó¦µÄµćĪ»ÓŚĒśĻßb”¢d¼äµÄijµć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļņ0.1 mol•L-1µÄCH3COOHČÜŅŗÖŠ¼ÓČėÉŁĮæĢ¼ĖįøĘ¹ĢĢ壬ČÜŅŗµÄpHŌö“ó | |
| B£® | ŹŅĪĀĻĀ£¬pH=4µÄNaHSO4ČÜŅŗÖŠ£¬Ė®µēĄė³öµÄH+ÅضČĪŖ1”Į10-10 mol•L-1 | |
| C£® | ÅØ¶Č¾łĪŖ0.1 mol•L-1µÄHCNČÜŅŗŗĶNaCNČÜŅŗµČĢå»ż»ģŗĻ£ØŗöĀŌĢå»ż±ä»Æ£©£¬ČÜŅŗÖŠc£ØHCN£©+c£ØCN-£©=0.1 mol•L-1 | |
| D£® | pHĻąĶ¬µÄ¢ŁNH4Cl”¢¢ŚNH4Al£ØSO4£©2”¢¢Ū£ØNH4£©2SO4ČżÖÖČÜŅŗµÄc£ØNH${\;}_{4}^{+}$£©£ŗ¢Ś£¼¢Ū£¼¢Ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
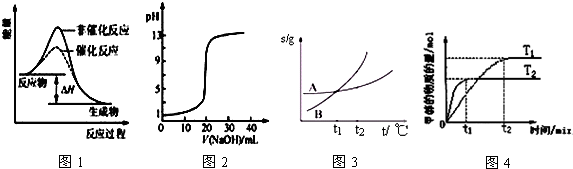
| A£® | Ķ¼1±ķŹ¾Ä³ĪüČČ·“Ó¦·Ö±šŌŚÓŠ”¢ĪŽ“߻ƼĮµÄĒéæöĻĀ·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ | |
| B£® | Ķ¼2±ķŹ¾0.1000 mol•L-1NaOHČÜŅŗµĪ¶Ø20.00mL0.1000 mol•L-1CH3COOHČÜŅŗĖłµĆµ½µÄµĪ¶ØĒśĻß | |
| C£® | Ķ¼3±ķŹ¾A”¢BĮ½ĪļÖŹµÄČܽā¶ČĖęĪĀ¶Č±ä»ÆĒéæö£¬½«tl”ꏱA”¢BµÄ±„ŗĶČÜŅŗ·Ö±šÉżĪĀÖĮt2”ꏱ£¬ČÜÖŹµÄÖŹĮæ·ÖŹżB=A | |
| D£® | Ķ¼4±ķŹ¾ŌŚĘäĖūĢõ¼žĻąĶ¬Ź±£¬·Ö±šŌŚT1”¢T2ĪĀ¶ČĻĀÓÉCO2ŗĶH2ŗĻ³É¼×“¼µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆĒéæö£¬ŌņCO2ŗĶH2ŗĻ³É¼×“¼ŹĒĪüČČ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| X | L²ćµē×ÓŹżŹĒK²ćµē×ÓŹżµÄ3±¶ |
| Y | ŗĖĶāµē×Ó²ćŹżµČÓŚŌ×ÓŠņŹż |
| Z | L²ćµē×ÓŹżŹĒK²ćŗĶM²ćµē×ÓŹżÖ®ŗĶ |
| W | ¹²ÓĆČż¶Ōµē×ÓŠĪ³ÉĖ«Ō×Ó·Ö×Ó£¬³£ĪĀĻĀĪŖĘųĢåµ„ÖŹ |
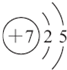 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾ŪŅŅĻ©ŹĒĪŽ¶¾øß·Ö×Ó»ÆŗĻĪļ£¬æÉÓĆ×÷Ź³Ę·°ü×° | |
| B£® | ŌŚČÕ³£Éś»īÖŠ£¬µē»ÆѧøÆŹ“ŹĒŌģ³ÉøÖĢśøÆŹ“µÄÖ÷ŅŖŌŅņ | |
| C£® | ĶĘ¹ćŹ¹ÓĆŠĀÄÜŌ“£¬æÉŅŌ¼õÉŁ¶žŃõ»ÆĢ¼µČĪĀŹŅĘųĢåµÄÅÅ·Å | |
| D£® | ČĖŌģĻĖĪ¬”¢ŗĻ³ÉĻĖĪ¬ŗĶ¹āµ¼ĻĖĪ¬¶¼ŹĒÓŠ»śøß·Ö×Ó»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖŠ¹ś¹Å“śĄūÓĆĆ÷·ÆČÜŅŗµÄĖįŠŌĒå³żĶ¾µ±ķĆęµÄĶŠā | |
| B£® | ·žÓĆ°¢Ė¾Ę„ĮÖ³öĻÖĖ®ŃīĖį·“Ó¦Ź±£¬ÓĆNaHCO3ČÜŅŗ½ā¶¾ | |
| C£® | ŹÆÓĶĮŃ½ā”¢ĆŗµÄøÉĮó”¢ÓńĆ×ÖĘ“¼”¢µ°°×ÖŹµÄ±äŠŌŗĶÄÉĆ×ŅųĮ£×ӵľŪ¼Æ¶¼ŹĒ»Æѧ±ä»Æ | |
| D£® | Č¼ĮĻµÄĶŃĮņĶѵŖ”¢SO2µÄ»ŲŹÕĄūÓĆŗĶNOxµÄ“ß»Æ×Ŗ»Æ¶¼ŹĒ¼õÉŁĖįÓź²śÉśµÄ“ėŹ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 100 mL1mol/LµÄNa2CO3ČÜŅŗÖŠŗ¬ÓŠ6.02”Į1022øöCO32- | |
| B£® | ×ćĮæĢś·ŪŌŚ0.05molCl2ÖŠ³ä·ÖČ¼ÉÕ£¬·“Ó¦Ź±×ŖŅĘ6.02”Į1022øöµē×Ó | |
| C£® | ½«4gNaOHČÜÓŚ100gÕōĮóĖ®£¬ĖłµĆČÜŅŗĪļÖŹµÄĮæÅØ¶ČŹĒ1mol/L | |
| D£® | ³£ĪĀĻĀ£¬½«9gĀĮʬĶ¶Čė500 mL 18.4 mol•L-1µÄĮņĖįÖŠ£¬²śÉśH2±Č11.2L¶ą |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com