
����Ŀ��(1)20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ��˵�������Ӧ��_________��������������������������Ӧ��NO2��CO��������_________������С������ ��������������������CO2��NO����������
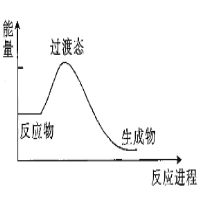
(2)��ij���Ϊ2L���ܱ������г���0.5mol NO2��1mol CO����һ�������·�����Ӧ��NO2+COCO2+NO��2minʱ�����������NO�����ʵ���Ϊ0.2mol����
�ٸö�ʱ���ڣ���CO2��ʾ��ƽ����Ӧ����Ϊ_________��
�ڼ���˷�Ӧ��5minʱ�ﵽƽ�⣬���ʱ����������������ʵ���Ϊ_________��
��������ʵ�ܹ�˵��������Ӧ�ڸ��������Ѿ��ﵽ��ѧƽ��״̬����_________��
A��������������������ֲ���
B��NO2�����ʵ���Ũ�Ȳ��ٸı�
C��NO2������������CO2�������������
D�������������ܵ����ʵ������ֲ���
���𰸡����� ���� 0.05molL��1min��1 1.5mol BC
��������
��1����ͼ��֪����Ӧ��NO2��CO������������������CO2��NO�����������÷�ӦΪ���ȷ�Ӧ��
��2������������г�����ʽ��

���ö�ʱ���ڣ���CO2��ʾƽ����Ӧ����Ϊ��![]() ��
��
����Ӧ��һ��ǰ���������ķ�Ӧ�����Է�Ӧ��5minʱ�ﵽƽ�⣬���ʱ����������������ʵ���=��Ӧǰ������������ʵ���=1.5mol��
����ѧƽ����ж���Ҫ�����ַ�����һ��v��=v�������DZ������䡣
A�������ڵ����巴Ӧǰ����ѭ�����غ㣬����������������Ǹ���ֵ�������ж��Ƿ�ﵽƽ��״̬��A����
B��NO2�����ʵ���Ũ���Ǹ����������ŷ�Ӧ�Ľ��в��ϱ仯���������ٸı�ʱ���÷�Ӧ�ﵽƽ��״̬��B��ȷ��
C��NO2������������Ӧ����CO2���������淴Ӧ������������ȷ��ϻ�ѧ������֮�ȣ���v��=v������Ӧ�ﵽƽ�⣬C��ȷ��
D����Ӧ��һ��ǰ���������ķ�Ӧ����ǰ�����ʵ�������ķ�Ӧ���������ʵ����Ǹ���ֵ�������ж��Ƿ�ﵽƽ��״̬��D����
��ѡBC��


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д� Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϡ�����ϡ����Ļ����Һ200 mL���������ۣ�����������������������ı仯��ͼ��ʾ����֪����ֻ����ԭΪNO���壩�����з���������ǣ�������
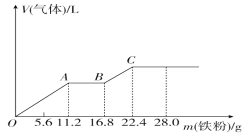
A.OA�β�������NO��AB�εķ�ӦΪFe��2Fe3��=3Fe2����BC�β���H2
B.A����Һ�е�����ΪFe(NO3)3��H2SO4
C.ԭ�������NO3-���ʵ���Ϊ0.2 mol
D.ԭ�������H2SO4�����ʵ���Ũ��Ϊ2 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ȳ����ż����Ӧ�ڿ������ͷ�����ϡ������ӵ���������Ҫ�о���ֵ����Ȳ������ż����ӦΪ 2CH��CH ![]() CH��CC��CH+H2����Ȳż����Ӧ�����������仯��ͼ�������ߢ���ʾ�����ߢ�Ϊ�ı�ijһ�����������仯������˵������ȷ���ǣ� ��
CH��CC��CH+H2����Ȳż����Ӧ�����������仯��ͼ�������ߢ���ʾ�����ߢ�Ϊ�ı�ijһ�����������仯������˵������ȷ���ǣ� ��
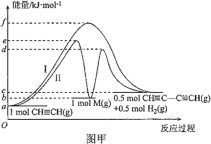
A.���ߢ�Ӧ����ܼ��ܴ�����������ܼ���
B.���ߢ�ı�������Ǽ����˴���
C.���ߢ��Ӧ�����£���һ����Ӧ�� ��H=+(b-a)kJ��mol-1
D.���ߢ��Ӧ�����£������ܷ�Ӧ���ʵĴ�С�ǵڶ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����f�����һ��������ʹҩ�����������Ʒ�ʪ�Թؽ��ס����ʪ�Թؽ����������Լ�����ij�о�С�鰴����·�ߺϳ�ҩ�ﱽ�f��ң�
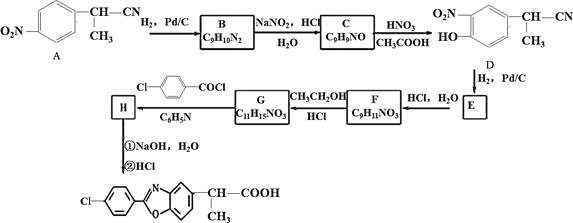
��֪��
![]()
![]()
��1��������F �еĺ��������ŵ�����Ϊ_____��
��2������˵����ȷ����_____��
A.������A �ܷ���ȡ����Ӧ���ӳɷ�Ӧ����ԭ��Ӧ
B.������ F ���������
C.������ C ���� FeCl3 ����ɫ�����Ժͼ�ȩ��һ�������·������۷�Ӧ
D ���f��ҵķ���ʽ��C16H11O3NCl
��3��������C �Ľṹ��ʽ_____��
��4��д��G��H �Ļ�ѧ����ʽ_____��
��5��д��������B ͬʱ��������������ͬ���칹��Ľṹ��ʽ_____��
�ٺ˴Ź������ױ����������� 4 ����ԭ�ӣ�
�ں��������ʾ�б������京����λ��ȡ������Ԫ��������N-H ����
��6��������ɱ�����ϩΪԭ���Ʊ�������A �ĺϳ�·��(������ͼ��ʾ�����Լ���ѡ)��___________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ɡ�λ�������һ���Ʊ���������: ����˵������ȷ����( )
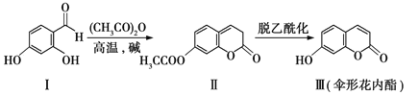
A. ����ܷ���ˮ�ⷴӦ
B. ���������ˮ��Ӧ
C. ���黯��������Ƿ���л��������FeCl3��Һ
D. �뻯�������������ࡢ��Ŀ����ͬ�Һ��б�����ͬ���칹����5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����ñ���Ũ���ᡢŨ���ᷢ����Ӧ��ȡ��������װ����ͼ��ʾ���ش��������⣺
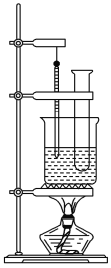
(1)��Ӧ����50��60����¶��½��У�ͼ�и���Ӧ����ȵķ�����ˮԡ���ȣ����ŵ���__________________________��_____________________��
(2) �÷�Ӧ�Ļ�ѧ����ʽ��_____________________����Ӧ���ͣ�_____________��
(3) ����װ�õ�ȱ�ݣ���ʵ����ܻᵼ�µIJ��������_____________________��
(4)��Ӧ��Ϻ�ȥ����ᣬ���ôֲ�Ʒ�����²������ƣ�
������ˮϴ�����ø�����������10%NaOH��Һϴ����ˮϴ
��ȷ�IJ���˳����_____________��
A���٢ڢۢܢ� B���ڢܢݢۢ� C���ܢڢۢ٢� D���ڢܢ٢ݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֡�
̼ | �� | Y | |
X | �� | Z |
�ش���������
��1��ZԪ�������ڱ��е�λ��Ϊ__________��
��2��Ԫ�����ڱ�����ZԪ��ͬ����ԭ�Ӱ뾶������(дԪ������)__________��������������Ӧ��ˮ���ﺬ�еĻ�ѧ������____________��
��3��������ʵ��˵��YԪ�صķǽ����Ա���Ԫ�صķǽ�����ǿ����___��
a��Y������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molY���ʱ�1molS�õ��Ӷ�
c��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
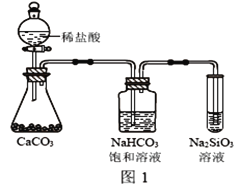
��4��������ͼʵ�飬����֤��̼�ķǽ����Ա�Xǿ������С�մ���Һ������__________�����������ӷ���ʽ�ǣ�__________________
��5����ˮ(D2O)����Ҫ�ĺ˹�ҵԭ�ϣ�����˵����������________��
a���(D)ԭ�Ӻ�����1������
b��1H��D����ͬλ��
c��H2O��D2O����ͬ��������
d��1H218O��D216O����Է���������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��1��18��Ԫ���е����֣�0.5molAԪ�ص����ӵõ�6.02��1023�����ӱ���ԭΪ����ԭ�ӣ�0.4g A��������ǡ����100mL0.2mol/L��������ȫ��Ӧ��Aԭ�Ӻ�������������������ȡ�B�ǵؿ��к������Ľ���Ԫ�ء�C�õ�һ�����Ӻ���벵ĵ��Ӳ�ṹ��ͬ��������������ˮ����Ϊ��Ȼ����ǿ�ĺ����ᡣDԪ���ǹ����л������ҪԪ�أ������ڲ��������������������һ�롣
(1)A�ĵ��ʿ���D�������������ȼ�յõ�һ�ְ�ɫ�����һ�ֺ�ɫ���壬��д���仯ѧ����ʽ______________________________��
(2)A��B��C�����Ӱ뾶�ɴ�С˳��Ϊ��______________��(�����ӷ��ű�ʾ)
(3)��10mLŨ��Ϊ1mol/L��B��C��Ԫ���γɵĻ������ˮ��Һ����ε���35mLŨ��Ϊ1mol/L�Ŀ�������Һ��������______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͼʾ���ó��Ľ��۲���ȷ����
A. ͼ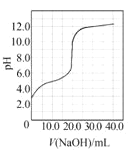 ����������0.1000 mol��L1NaOH��Һ�ζ�20.00 mL 0.1000 mol��L1ijһԪ��HX�ĵζ����ߣ�˵��HX��һԪǿ��
����������0.1000 mol��L1NaOH��Һ�ζ�20.00 mL 0.1000 mol��L1ijһԪ��HX�ĵζ����ߣ�˵��HX��һԪǿ��
B. ͼ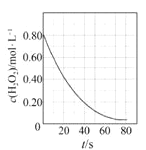 ��������H2O2���ֽ�ų������ķ�Ӧ��c(H2O2 )�淴Ӧʱ��仯�����ߣ�˵�����ŷ�Ӧ�Ľ���H2O2�ֽ�������С
��������H2O2���ֽ�ų������ķ�Ӧ��c(H2O2 )�淴Ӧʱ��仯�����ߣ�˵�����ŷ�Ӧ�Ľ���H2O2�ֽ�������С
C. ͼ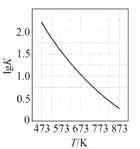 ��CO(g)+H2O(g)
��CO(g)+H2O(g)![]() CO2(g)+H2(g)��ƽ�ⳣ���뷴Ӧ�¶ȵĹ�ϵ���ߣ�˵���÷�Ӧ�Ħ�H<0
CO2(g)+H2(g)��ƽ�ⳣ���뷴Ӧ�¶ȵĹ�ϵ���ߣ�˵���÷�Ӧ�Ħ�H<0
D. ͼ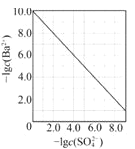 ����������Na2SO4��ȥ��Һ��Ba2+�ﵽ�����ܽ�ƽ��ʱ����Һ��c(Ba2+ )��c(SO42)�Ĺ�ϵ���ߣ�˵����Һ��c(SO42 )Խ��c(Ba2+ )ԽС
����������Na2SO4��ȥ��Һ��Ba2+�ﵽ�����ܽ�ƽ��ʱ����Һ��c(Ba2+ )��c(SO42)�Ĺ�ϵ���ߣ�˵����Һ��c(SO42 )Խ��c(Ba2+ )ԽС
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com