


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011年高考化学总复习30分钟限时训练:专题9 电化学基础 题型:022
利用太阳光分解水制氢是未来解决能源危机的理想方法之一.某研究小组设计了如图所示的循环系统实现光分解水制氢.反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe2+等可循环使用.
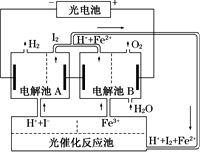
(1)写出下列反应中的离子方程式:
电解池A:________;
电解池B:________;
光催化反应池:________.
(2)若电解池A中生成3.36 L H2(标准状况),电解池B中生成Fe2+的物质的量为________.
(3)若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol/L和b mol/L,光催化反应生成Fe3+的速率为c mol/min,循环系统中溶液的流量为Q(流量为单位时间内流过的溶液体积).试用所给字母的代数式表示溶液的流量Q=________.
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省周口市高一(上)第一次月考化学试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com