
下列元素周期表的区域中,含有较多用于制催化剂、耐高温耐腐蚀的材料元素的是( )
A. 金属元素和非金属元素分界线附近
B. 过渡元素
C. 左下方区域的金属元素
D. 右上方区域的非金属元素
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:
Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.用小苏打治疗胃酸过多:
HCO +H+===H2O+CO2↑
+H+===H2O+CO2↑
C.实验室用浓盐酸与MnO2反应制Cl2:
MnO2+2H++2Cl- Cl2↑+Mn2++H2O
Cl2↑+Mn2++H2O
D.用FeCl3溶液腐蚀印刷电路板:
Fe3++Cu===Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸镍铵[(NH4)xNiy(SO4)m·nH2O]可用于电镀、印刷等领域。某同学为测定硫酸镍铵的组成,进行如下实验:①准确称取2. 3350 g 样品,配制成100. 00 mL 溶液A;②准确量取25. 00 mL 溶液A,用0. 04000 mol·L-1 的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+ ),消耗EDTA 标准溶液31. 25 mL;③另取25. 00 mL溶液A,加足量的NaOH 溶液并充分加热,生成NH3 56. 00 mL(标准状况)。
(1)若滴定管在使用前未用EDTA 标准溶液润洗,测得的Ni2+含量将 (填“偏高”、或“偏低”或“不变”)。
(2)氨气常用 检验,现象是 。
(3)通过计算确定银硫酸镍铵的化学式(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气.下列说法正确的是( )
|
| A. | 甲烧杯中放入锌的质量比乙烧杯中放入锌的质量小 |
|
| B. | 两烧杯中参加反应的锌等量 |
|
| C. | 甲烧杯中的酸过量 |
|
| D. | 反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
硒(Se)被科学家称之为人体微量元素中的“防癌之王”,同时也是“心脏的守护神”“肝病的天敌”,对人体具有良好的保健作用。已知硒为第四周期、与氧同一族,根据它在周期表中的位置推测,硒不可能具有的性质为( )
A.硒也有两种氧化物,分别为SeO2和SeO3两种
B.硒化氢属于共价化合物,比硫化氢稳定
C.硒化氢的水溶液显弱酸性
D.硒单质的非金属性比氧弱
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,一个密闭容器中;加入1molN2和3moH2发生

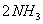 反应,则下列叙述正确的是( )
反应,则下列叙述正确的是( )
A.若速率V(N2): V(H2) : V(NH3) = 1:3:2 ,则该反应反应达到了 平衡状态
B. 反应开始时,若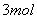
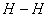 键断裂,则有2mol N—H 键生成
键断裂,则有2mol N—H 键生成
C. 改变条件可以改变该反应限度,会使反应物完全反应
D. 当反应混合物各组分的物质的量浓度不再改变,该反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2、NO是大气污染物。吸收SO2 和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中生成HSO3-的离子方程为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如右图所示。

①下列说法正确的是 (填字母序号)。
a.pH=8时,溶液中c(HSO3-) < c(SO32-)
b.pH=7时,溶液中c(Na+) =c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式 。
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。

①生成Ce4+的电极反应式为 。
②生成Ce4+从电解槽的 (填字母序号)口流出。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于烃的性质的说法中正确的是( )
A.苯和甲苯都能与硝酸发生苯环上的取代反应
B.苯和甲苯使酸性高锰酸钾溶液褪色
C.苯和己炔都能使溴的四氯化碳溶液褪色
D.苯和乙烷与卤素单质发生取代反应都需要铁作催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com