
分析 苹果酸是一种烃的含氧衍生物,相对分子质量小于140,且C、H质量分数依次为35.82%和4.47%,则苹果酸分子中O原子最大数目=$\frac{140×(1-35.82%-4.47%)}{16}$=5.2,0.l mol苹果酸与足量NaHCO3溶液反应能产生4.48L CO2(标准状况),二氧化碳的物质的量为0.2mol,则1mol苹果酸含2mol-COOH,与足量Na反应放出3.36L 气体,生成氢气为0.15mol,则苹果酸还含有1个-OH,故苹果酸分子含有5个O原子,则苹果酸相对分子质量为=$\frac{5×16}{1-35.82%-4.47%}$=134,去掉2个-COOH、1个-OH后剩余总式量为134-45×2-17=27,应为-C2H3-,可以确定分子式,结合苹果酸分子结构中不含碳的支链确定苹果酸结构简式.
解答 解:苹果酸是一种烃的含氧衍生物,相对分子质量小于140,且C、H质量分数依次为35.82%和4.47%,则苹果酸分子中O原子最大数目=$\frac{140×(1-35.82%-4.47%)}{16}$=5.2,0.l mol苹果酸与足量NaHCO3溶液反应能产生4.48L CO2(标准状况),二氧化碳的物质的量为0.2mol,则1mol苹果酸含2mol-COOH,与足量Na反应放出3.36L 气体,生成氢气为0.15mol,则苹果酸还含有1个-OH,故苹果酸分子含有5个O原子,则苹果酸相对分子质量为=$\frac{5×16}{1-35.82%-4.47%}$=134,去掉2个-COOH、1个-OH后剩余总式量为134-45×2-17=27,应为-C2H3-,可以确定苹果酸分子式为C4H6O5,
故答案为:C4H6O5;
(2)苹果酸分子结构中不含碳的支链,苹果酸的结构简式为:HOOCCH2CH(OH)COOH,
故答案为:HOOCCH2CH(OH)COOH.
点评 本题考查有机物的推断,关键是判断苹果酸分子中含有羧基、羟基数目,题目难度中等.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 卤素与碱金属容易形成离子键 | |
| B. | CH4分子中只有共价键 | |
| C. | 碳元素一般容易生成含共价键的共价化合物 | |
| D. | 在NaOH中只有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
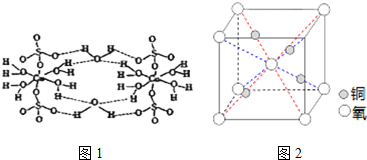
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第2周期与第3周期元素从左到右,最高正化合价均从+1逐渐增大至+7,0族元素一般是0价 | |
| B. | 3个长周期所含元素种数相同 | |
| C. | 不同主族的3、4周期元素原子序数的差可能不同 | |
| D. | 同周期从左到右,非金属元素含氧酸的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol组成为C2H6O的有机物,所含C-H键数目可能为0.5NA | |
| B. | 8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| C. | 0.1 mol N2与0.3 mol H2在密闭容器中,在催化剂作用下充分反应,生成氨分子数为0.2NA | |
| D. | 标准状况下,22.4 L HF所含的分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:浓硝酸大于稀硝酸 | |
| B. | 与相同质量的铜(反应完全)反应中转移的电子总数相同 | |
| C. | 与锌反应:前者生成NO2,后者生成H2 | |
| D. | 与铜反应:前者生成气体颜色深,后者生成气体颜色浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,32gO2含有2nA个氧原子 | |
| B. | 1mol Na2O2与足量水反应,转移2nA个电子 | |
| C. | 1L0.1mol•L-1Na2CO3溶液中含有0.1nA个CO${\;}_{3}^{2-}$ | |
| D. | 常温常压下,22.4LCH4中含有nA个CH4分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5×10-3 | B. | 5×10-6 | C. | 2.6×10-4 | D. | 无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com