
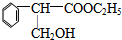 ,F的结构简式为
,F的结构简式为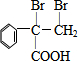 .
.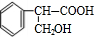 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$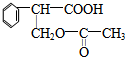 +H2O;②A→E:2
+H2O;②A→E:2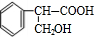 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O.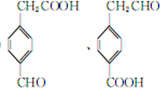 .
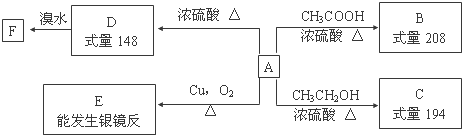
. 分析 某芳香族化合物A,完全燃烧只生成二氧化碳和水,说明A中只含C、H、O三种元素.A能被氧气氧化生成E,E能发生银镜反应,说明A中含有醇羟基,且-OH相连的C原子上含有2个H原子,A能与乙醇反应,说明A中含有羧基.A在浓硫酸、加热条件下生成D,D与溴水发生反应,D中含有C=C双键,故A生成D的反应为醇的消去反应,D的式量为148,假设D中含有1个苯环、1个羧基,故剩余基团的式量为148-45-77=26,故剩余组成为C2H2,结合A中-OH相连的C原子上含有2个H原子,A的苯环上只有一个取代基,故D为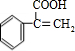 ,A为
,A为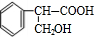 ,E为
,E为 .A与乙酸发生酯化反应生成B,B为
.A与乙酸发生酯化反应生成B,B为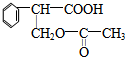 ,A与乙醇发生酯化反应生成C,C为
,A与乙醇发生酯化反应生成C,C为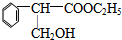 ,以此解答该题.
,以此解答该题.
解答 解:某芳香族化合物A,完全燃烧只生成二氧化碳和水,说明A中只含C、H、O三种元素.A能被氧气氧化生成E,E能发生银镜反应,说明A中含有醇羟基,且-OH相连的C原子上含有2个H原子,A能与乙醇反应,说明A中含有羧基.A在浓硫酸、加热条件下生成D,D与溴水发生反应,D中含有C=C双键,故A生成D的反应为醇的消去反应,D的式量为148,假设D中含有1个苯环、1个羧基,故剩余基团的式量为148-45-77=26,故剩余组成为C2H2,结合A中-OH相连的C原子上含有2个H原子,A的苯环上只有一个取代基,故D为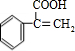 ,A为
,A为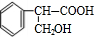 ,E为
,E为 .A与乙酸发生酯化反应生成B,B为
.A与乙酸发生酯化反应生成B,B为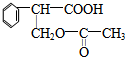 ,A与乙醇发生酯化反应生成C,C为
,A与乙醇发生酯化反应生成C,C为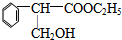 ,
,
(1)B是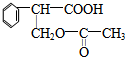 ,含有酯基可以发生水解反应,含有羧酸可以发生取代反应,含有苯环,可以发生加成反应,不能发生消去反应与加聚反应,
,含有酯基可以发生水解反应,含有羧酸可以发生取代反应,含有苯环,可以发生加成反应,不能发生消去反应与加聚反应,
故答案为:①②;
(2)由以上分析可知C为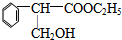 ,D为
,D为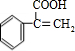 ,含有碳碳双键,与溴水发生加成反应生成F为
,含有碳碳双键,与溴水发生加成反应生成F为 ,
,
故答案为: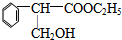 ;
; ;
;
(3)A→B的方程式为:CH3COOH+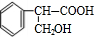 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$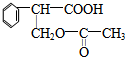 +H2O,
+H2O,
A为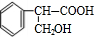 含有羟基,在铜催化作用下生成
含有羟基,在铜催化作用下生成 ,反应的方程式为2
,反应的方程式为2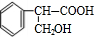 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O,
+2H2O,
故答案为:CH3COOH+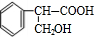 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$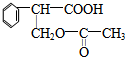 +H2O;2
+H2O;2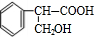 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O;
+2H2O;
(4)对应的同分异构体中:①与E具有相同的官能团,应含有醛基,②苯环上一氯取代物只有二种,说明苯环含有2个取代基,且位于对位的位置,则对应额同分异构体可能为 ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及计算能力,涉及结构简式的判断、反应方程式的书写、同分异构体的确定等知识点,难点的同分异构体的书写.


科目:高中化学 来源: 题型:选择题
| A. | 分散质粒子直径在1~100nm之间 | B. | 可用丁达尔效应区别这两种物质 | ||
| C. | 能用过滤的方法将它们分离 | D. | 都呈红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
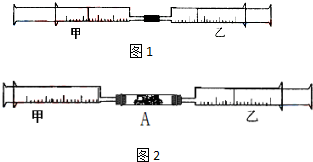 如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).
如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 40mL HCl | 40mL NH3 | 产生白烟 |
| 2 | 40mL Cl2 | 10mL 水 | 剩余气体为20mL |
| 3 | 30mL NO | 15mL O2 | |
| 4 | 20mL AlCl3溶液 | 10mL NaOH溶液 | 生成白色沉淀,后消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2中混有少量SO3,通过足量浓硫酸,收集气体 | |
| B. | HNO3溶液中混有少量H2SO4,加入适量BaCl2溶液,再过滤 | |
| C. | 提取溴水中的溴,可用加入乙醇萃取的方法 | |
| D. | 检验溶液中是否含有Fe2+,向溶液中滴入氯水后,再滴加KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正丁烷和异丁烷的一氯取代物都只有两种,它们的沸点也相同 | |
| B. | 乙烯分子与苯分子都能与H2发生加成反应,说明二者均含碳碳双键 | |
| C. | 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 | |
| D. | 乙醛加入Cu(OH)2粉末并加热可看到红色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
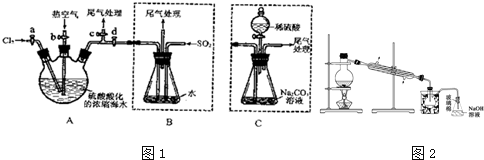
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
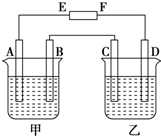 在图中,E和F分别为电源两极;甲烧杯中盛有100mL 0.2mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.15mol•L-1 CuCl2溶液,A、B、C、D均为石墨电极,如果电解一段时间后,发现B极增重1.08g,则
在图中,E和F分别为电源两极;甲烧杯中盛有100mL 0.2mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.15mol•L-1 CuCl2溶液,A、B、C、D均为石墨电极,如果电解一段时间后,发现B极增重1.08g,则查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com