
(1) 、—CH3、
、—CH3、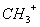 都是重要的有机反应中间体,有关它们的说法正确的是_________________
都是重要的有机反应中间体,有关它们的说法正确的是_________________
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.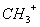 中的碳原子采取sp2杂化,所有原子均共面
中的碳原子采取sp2杂化,所有原子均共面
E.两个—CH3或一个 和一个
和一个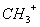 结合均可得到CH3CH3
结合均可得到CH3CH3
(2)锌是一种重要的金属,锌及其化合物有着广泛的应用。
①指出锌在周期表中的位置:第________周期,第________族,属于________区。
②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。葡萄糖分子中碳原子杂化方式有___________;写出基态Zn原子的电子排布式___________________。
(9分) (1)C、D、E (2)①四; ⅡB; ds
②sp2、sp3; 1s22s22p63s23p63d104s2或[Ar]3d104s2 【(2)②2分,其余每空1分】
【解析】
试题分析:(1)甲烷失去氢原子后应该电中性的,A不正确;原子数和电子数分别都相等的是等电子体,微粒中电子数不相等,不能互为等电子体,B不正确,C正确;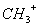 中的碳原子含有(4-1-3×1)÷2=0对孤对电子,所以
中的碳原子含有(4-1-3×1)÷2=0对孤对电子,所以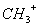 中的碳原子采取sp2杂化,所有原子均共面,D正确;选项E也正确的,答案选CDE。
中的碳原子采取sp2杂化,所有原子均共面,D正确;选项E也正确的,答案选CDE。
(2)①锌的原子序数是30,位于第四周期第ⅡB族,属于ds区。
②葡萄糖分子中碳原子既可用形成单键,也可用形成双键,所以既有sp2杂化,也有sp3杂化。根据构造原理可知,基态Zn原子的电子排布式1s22s22p63s23p63d104s2或[Ar]3d104s2。
考点:考查分子的空间构型、杂化轨道、等电子体、元素在周期表中的位置以及核外电子排布
点评:该题是中等难度的试题,试题基础性强,难易适中,贴近高考。在注重对基础知识考查与巩固的同时,主要是侧重对学生解题能力与技巧的培养和训练,有利于培养学生的灵活运用基础知识解决实际问题的能力,也有助于提高学生的创新思维能力和发散思维能力,提高学生的应试能力。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省昭觉中学高二10月月考化学试卷(带解析) 题型:填空题
(1) 、—CH3、
、—CH3、 都是重要的有机反应中间体,有关它们的说法正确的是_________________
都是重要的有机反应中间体,有关它们的说法正确的是_________________
| A.它们均由甲烷去掉一个氢原子所得 |
| B.它们互为等电子体,碳原子均采取sp2杂化 |
| C.CH与NH3、H3O+互为等电子体,几何构型均为三角锥形 |
D. 中的碳原子采取sp2杂化,所有原子均共面 中的碳原子采取sp2杂化,所有原子均共面 |
 和一个
和一个 结合均可得到CH3CH3
结合均可得到CH3CH3查看答案和解析>>
科目:高中化学 来源:2010年海南省海口市高三下学期高考调研(一)化学试题 题型:填空题
(20分)
(I)多项选择题(6分)
CH3+、CH3-、CH3-都是重要的有机反应中间体,有关它们的说法正确的是 。
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个CH3-或一个CH3+和CH3-结合均可得到CH3CH3
(II)(14分)
锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置: 周期, 族, 区。
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式 ;葡萄糖分子中碳原子杂化方式有 。
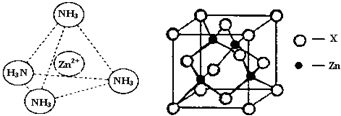
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于 (填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在左下图中表示[Zn(NH3)4]2+中Zn2+与N之间的化学键。


(4)右上图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为 ;该化合物的晶体熔点比干冰高得多,原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com